Биохимия функциональная. Функциональная биохимия Функциональная биохимия кратко
1. Введение в биохимию.
1. 1. Биосфера и биологический круговорот веществ и энергии. Пищевые цепи. Автотрофы и гетеротрофы. Симбмоз. Прокариоты и эукариоты. Строение пр о- и эукариотической клетки. Функции органелл и цитоплазмы клетки.
1. 2. Химический состав живых систем. Основные классы биоорганических соединений. " Органический алфавит" жизни. Биологические функции воды. Основной (первичный) и вторичный метаболизм. Катаболизм и анаболизм. Основные пути регуляции биохимических процессов.
1. 3. Энергетический обмен клетки. Макроэргические соединения. Природа макроэргической связи. АТФ и другие фосфорилированные соединения. Энергетический заряд клетки. Пути использования энергии, запасаемой в высокоэнергетических соединениях.
2. Углеводы.
2. 1. Структура и биологические функции.
Моносахариды: альдозы и кетозы. Стереоизомерия. Способы изображения (проекции Фишера и Хеоурса, конформационные формулы). Биологические функции моносахаридов.
Олигосахариды - структура и биологические функции.
Полисахариды: структура и биологические функции полисахаридов животных и грибов (гликогена и хитина), растений (крахмала, целлюлозы, инулина, пектинов, гемицеллюлоз - маннанов, галактанов и ксиланов), водорослей (агар-агара, альгиновых кислот) и бактерий (декстрна). Пептидогликаны бактерий и гликопротеиды животных. Гликозаминогликаны и протеогликаны.
2. 2. Гликолиз и гликогенолиз. Гликолиз - центральный путь катаболизма глюкозы. Стадии и подстадии гликолиза. " Запусковые " реакции и этапы запасания энергии. Субстратное фосфарилирование. Необратимые стадии гликолиза. " Кислородная задолженность". Пути вовлечения в гликолиз различных ди - и моносахаридов. Гликогенолиз. Регуляция гликолиза и гликонеогенеза. Спиртовое и молочнокислое брожение.
2. 3. Цикл лимонной кислоты и глиоксалатный цикл.
Пируватдегидрогеназный комплекс ферментов. Коферменты и кофакторы комплекса. Цикл лимонной кислоты. Регуляция окислительного декарбоксилирования пирувата и цикла лимонной кислоты. Анаплеротические реакции. Глиоксилатный цикл и его функции.
2. 4. Электрон-транспортная цепь и окислительное фосфорилирование. Внутриклеточная локализация процессов гликолиза, цикла лимонной кислоты и электрон-транспортной системы. Структура митохондрий и челночные системы. Коллекторная функция NADH и FADH 2. Четыре комплекса электрон-транспортной цепи. Флавинмононуклеотид. Хемиосмотическая гипотеза и окислительное фосфорилирование. Структура и механизм действия АТР-синтетазы.
2. 5. Глюконеогенез. Превращение пирувата в фосфоенолпируват. Сходства и различия гликолиза и глюконеогенеза. Реципкорная регуляция гликолиза и глюконеогенеза. " Холостые циклы" в углеводном обмене и их роль. Синтез гликогена. Реципкорная регуляция гликоген-синтетазы и гликоген-фосфорилазы.
2. 6. Фотосинтез и фотосинтетическое фосфорилирование. Разнообразие фотосинтетиков и доноров водорода при фотосинтезе. Световая и темновая стадии фотосинтеза. Структура и назначение хлорофиллов и каратиноидов. Два типа фотохимических систем и их взаимодействие. Z -схема и циклическое фосфорилирование. Электрон-транспортная система хлоропластов.
Циклическое фосфорилирование. Общее уравнение фотосинтеза. Фиксация двуокиси углерода. Представление о цикле Кальвина.
3. Липиды.
3. 1. Структура и функии липидов. Классификация липидов.
Триглицеролы. Строение и функции триглицеролов. Насыщенные (лауриновая, миристиновая, пальмитиновая, стеариновая и арахиновая) и ненасыщенные (пальмитолеиновая, олеиновая, линолевая, линолеиновая и арахидоновая) кислоты. Состав растительных и животных жиров. Воска. Фосфолипиды. Фосфатидная кислота. Фосфатидилсерин, фосфатидилэтаноламин (кефалин), фосфатидилхолин (лецитин), кардиолипин. Стероиды. Состав и структура клеточных мембран. Жидко-мозаичная модель Сингера-Никольсона. Липопротеины.
3. 2. Окисление жирных кислот. Механизм активации, переноса жирных кислот через внутреннюю мембрану митохондрий. р -Окисление жирных кислот до ацетил-СоА. Первая и вторая (до углекислого газа и воды) стадии окисления жирных кислот. Особенности окисления ненасыщенных жирных кислот и жирных кислот с нечетным числом атомов, углерода. Функции биотина и коэнзимной формы витамина В 12. Образование кетоновых тел в печени и их использование в мышцах.
3. 3. Биосинтез жирных кислот. Челночный механизм переноса ацетильных групп из матрикса митохондрий в цитозоль. Образование малонил-СоА. Строение и механизм действия синтетазы жирных кислот. Стадии синтеза жирных кислот. Сходства и различия между окислением и синтезом жирных кислот.
3. 4. Синтез и гидролиз жиров и фосфолипидов. Образование ди - и триацилглицерола. Реутилизация холина и синтез лецитина de novo
. Основные этапы синтеза холестерола.
4. Азотсодержащие соединения.
4. 1. Аминокислоты: строение и биологические функции. Понятие о заменимых и незаменимых аминокислотах. Взаимосвязь аминокислот с метаболитами гликолиза и цикла лимонной кислоты. Механизм реакции переаминирования. Перидоксаль и перидоксамин. Глутаминаза и глутаминсинтетаза.
4. 2. Расщепление и биосинтез аминокислот. Токсичность аммиака и орнитиновый цикл. Аммин о -, урео - и урикотелические организмы. Глюкогенные и кетогенные аминокислоты. Пути распада и синтеза аминокислот, сходства и различия катаболических и анаболических путей. Роль тетрагидрофолиевой кислоты.
4. 3. Строение и биологические функции азотистых оснований.
5. Витамины
5. 1. Жирорастворимые витамины (A, D, Е, К).
5. 2. Водорастворимые витамины (В 1 В 2 , В 3 , В 5 , В 6 , В 12 , С, липоевая кислота, убихинон, биотин, фолиевая кислота).
Основная
1. А. Ленинджер Основы биохимии, в 3-х т. М.: Мир, 1985.
2. В. Эллиот, Д. Эллиот Биохимия и молекулярная биология. М.: Изд-во НИИ биомедицинской химии РАМН, 2000.
Дополнительная
1. Д. Мецлер Биохимия, в 3-х т. М.: Мир, 1980.
2. Л. Страйер Биохимия, в 3-х т. М.: Мир, 1985.
3. Р. Мари, Греннер Д., Мейес П., Родуэлл П. Биохимия человека, в 2-х т. М.: Мир, 1993.
4. Д. Г. Кнорре, С. Д. Мызина Биологическая химия. М.: Высшая школа, 1998.
Программа составлена
проф. Гладилиным А. К
Раздел Б., изучающий химические превращения, лежащие в основе функций органов, тканей и организма в целом.
- - биологическая химия, наука о химич. составе живой материи и о химич. процессах, происходящих в живых организмах и лежащих в основе их жизнедеятельности. Б. слагается из статической Б., занимающейся...
Биологический энциклопедический словарь
- - наука, изучающая входящие в состав организмов хим. в-ва, их структуру, распределение, превращения и функции...
Сельско-хозяйственный энциклопедический словарь
- - биологическая химия, наука, изучающая химические процессы, происходящие в раст. и у жив., т. е. тот круговорот химических элементов, к-рый последние проходят сначала в растительном организме при построении...
Сельскохозяйственный словарь-справочник
- - биологическая химия, наука, изучающая химич...
Ветеринарный энциклопедический словарь
- - междисциплинарная наука, изучает химический состав и структуру веществ, содержащихся в живых организмах, пути и способы регуляции их метаболизма, а также энергетическое обеспечение процессов, происходящие в клетке и...
Начала современного Естествознания
- - I Биохи́мия биологическая химия - наука о химическом составе живых систем всех уровней организации, о химических процессах, лежащих в основе их развития и деятельности, происходящих в целостном организме, в...
Медицинская энциклопедия
- - изучает входящие в состав организмов хим. в-ва, их структуру, распределение, превращения и функции. Первые сведения по Б. связаны с хоз. деятельностью человека и медициной...
Естествознание. Энциклопедический словарь
- - наука, изучающая химическую природу веществ, входящих в состав живых организмов, и химические процессы, лежащие в основе их жизнедеятельности...
Большой медицинский словарь
- - наука, изучающая состав и химические процессы, происходящие в живых организмах...
Экологический словарь
- - учение об обмене материи в живых телах...
Энциклопедический словарь Брокгауза и Евфрона
- - I Биохи́мия биологическая химия, наука, изучающая состав организмов, структуру, свойства и локализацию обнаруживаемых в них соединений, пути и закономерности их образования, последовательность и механизмы...
Большая Советская энциклопедия
- - наука о химических веществах, входящих в состав организмов, их структуре, распределении, превращениях и функциях, а также о химических процессах, лежащих в основе жизнедеятельности...
Современная энциклопедия
- - изучает входящие в состав организмов химические вещества, их структуру, распределение, превращения и функции. Первые сведения по биохимии связаны с хозяйственной деятельностью человека и медициной...
Большой энциклопедический словарь
- - ...
Орфографический словарь-справочник
- - Р., Д., Пр....
Орфографический словарь русского языка
"биохимия функциональная" в книгах
Биохимия атеросклероза
автораБиохимия атеросклероза
Из книги Биологическая химия автора Лелевич Владимир ВалерьяновичБиохимия атеросклероза Атеросклероз – это патология, характеризующаяся появлением атерогенных бляшек на внутренней поверхности сосудистой стенки. Одна из основных причин развития такой патологии – нарушение баланса между поступлением холестерола с пищей, его
Биохимия квашения
автора Гладков Сергей МихайловичБиохимия квашения
Из книги Умное сыроедение. Пища для тела, души и духа автора Гладков Сергей МихайловичБиохимия богов
Из книги Древние боги - кто они автора Скляров Андрей ЮрьевичБиохимия богов Однако кровь на основе гемоцианина имеет не только некоторые преимущества, но и серьезные недостатки. И прежде всего в том, что касается транспортных свойств - только по отношению не к кислороду, а к углекислому газу. Но здесь нам сначала придется
Биохимия депрессии
Из книги Смертельные эмоции автора Колберт ДонБиохимия депрессии Современные научные методы позволяют исследовать структуру и работу различных участков мозга живого человека и выявлять нарушения, ведущие к психическим расстройствам.Нейрофизиолог и детский психиатр Даниэль Амен много лет занимается изучением
Биохимия
БСЭ«Биохимия»
Из книги Большая Советская Энциклопедия (БИ) автора БСЭБИОХИМИЯ ПСИХОЗОВ
Из книги Психиатрия. Руководство для врачей автора Цыганков Борис ДмитриевичБИОХИМИЯ ПСИХОЗОВ Предположения о выделении «особого эфира» в нервных окончаниях сделал еще В. Куллен (1776), который в связи с этим считал, что все болезни являются нервными, и предложил для их обозначения термин «неврозы». Успехи нейронаук позволили в настоящее время
3.8.3. Биохимия организма
Из книги Нарушение углеводного обмена автора Монастырский Константин3.8.3. Биохимия организма Развитие, рост и регенерация живых тканей начинается в момент зачатия и продолжается до последнего вздоха. Для бесперебойного деления всех клеток человек нуждается в воде, белках, жирах, минералах и микроэлементах приблизительно в тех же
БИОХИМИЯ КОЖИ
Из книги Кожные и венерические болезни автора Иванов Олег ЛеонидовичБИОХИМИЯ КОЖИ Кожа человека представляет собой очень сложную структуру, построенную из различных типов химических веществ. Это интегрированная система с взаимодействующими между собой химическими компонентами. Кожа человека на 69-73% состоит из воды. Различные слои
Биохимия при анемии
Из книги Всё, что нужно знать о своих анализах. Самостоятельная диагностика и контроль за состоянием здоровья автора Пигулевская Ирина СтаниславовнаБиохимия при анемии Кроме общего анализа крови при анемии при необходимости врач назначает и биохимические анализы: железо в сыворотке крови (см. раздел «Электролиты крови»), железосвязывающая способность сыворотки крови (ЖСС), трансферрин, ферритин. Совокупность
Биохимия и биофизика
Из книги Тайная мудрость человеческого организма автора Залманов Александр СоломоновичБиохимия и биофизика Имя первой науки нисколько не соответствует предмету, содержащемуся в этом разделе химии. Биохимия, собственно, означает: химия жизни, химия жизненных явлений. Однако ни химики, ни физиологи не в состоянии дать какое-нибудь объяснение жизни.
Биохимия зависимости
Из книги Я был бы счастлив, если бы не... Избавление от любого рода зависимостей автора Фрейдман ОлегБиохимия зависимости Часто пациенты спрашивают: «Почему это случилось именно со мной? Ведь другие живут так же как и я: неправильно питаются, не соблюдают режим, периодически употребляют алкоголь (наркотики), а остаются стройными (не становятся наркоманами, не испытывают
13 Биохимия
Из книги Ментальная химия: Наука исполнения желаний автора Энел Чарльз13 Биохимия Биохимия - это наука, занимающаяся процессами жизнедеятельности организма. Опирается она на клеточную теорию и принцип бесконечной делимости материи. В биохимии нашла отражение концепция гомеопатической дозы. Согласно этой концепции, доза лекарства должна
Строение мышц. Главные компоненты сократительных систем. Мышцы составляют около половины массы всего
тела.
Основная динамическая функция мышц- обеспечить
подвижность путем сокращения и последующего
расслабления. Мышечная клетка состоит из
отдельных волокон. В клетке имеются миофибриллы
– организованные пучки белков, расположенных
вдоль клетки. Миофибриллы построены из
филаментов – белковых нитей двух типов – толстых
и тонких филаментов. Основным белком толстых
филаментов является миозин, тонких – актин.
Функциональная единица миофибриллы – саркомер,
участок миофибриллы между двумя Z пластинами.
Строение мышц. Главные компоненты сократительных систем.
Саркомер включает пучок миозиновых нитей,серединой прикрепленные к М-пластине (М-линия),пучки
актиновых нитей прикреплены к Z-пластине.
Сокращение мышц есть результат укорочения каждого
саркомера, путем вдвигания актиновых нитей между
миозиновыми в направлении М-линии. Максимальное
укорочение достигается тогда, когда Z-пластины
приближаются вплотную к концам мизиновых нитей.
Z
M
Z
Механизм сокращения
Миозин – белок миозиновых нитей содержит двеидентичные цепи, скрученные между собой, N –концы
имеют глобулярную форму, образуя головки молекул.
Эти головки имеют высокое сродство к АТФ и
обладают каталитической активностью –
катализируют расщепление АТФ.
Актин в тонких филаментах связан с белком
тропонином, который имеет Са++-связывающие
центры. Актин - центры, связывания с миозином.
Сокращение мышцы вызывается потенциалом действия
нервного волокна и происходит за счет энергии АТФ.
Потенциал действия вызывает поступление Са++ из
ретикулома в цитозоль клетки.
Механизм мышечного сокращения
Са++А
А. Са++ связывается с тропонином
актиновых нитей и открывается в актине центр
связывания с миозином; Миозин связан с АТФ
Б
Б. Сцепление актиновых и миозиновых
нитей, при этом активируется АТФ-азный центр
миозина, головка миозина катализирует
гидролиз АТФ;
В
В. АДФ и Р покидают головку миозина, это
приводит к изменению конформации ее и она
поворачивается к линии М, увлекая
продвижение и актина. Происходит
сокращение.
Г
Г. К миозину присоединяется новая молекула
АТФ и связь между нитями нарушается.
Сотни миозиновых молекул работают
одновременно продвигая актиновый филомент
Мышечное сокращения. Условия.
Сила сокращения зависит от количества миозиновыхголовок, включенных в работу, а значит, и от
количества молекул АТФ.
Покоящаяся мышца эластична. Головка миозина
связана с АТФ.
Сокращенная мышца неэластична, напряжена.
Растяжению препятствует связь между актином и
миозином.
Ригидность возникает при сильном снижении
концентрации АТФ (условия гипоксии). В этих
условиях большое количество головок миозина
остается связанными с актином, т.к. для выхода из
этого состояния требуется присоединение АТФ к
миозину.
Источники энергии (АТФ)для мышечного сокращения.
Мышца, работающая с максимальной активностью потребляетэнергии в сотни раз больше, чем покоящаяся, а переход от
состояния покоя к работе происходит за доли сек. В связи с этим
для мышцы в отличие от других органов необходимы механизмы
изменения скорости синтеза АТФ в очень широких пределах
(исключение сердечной мышцы).
Общее содержание АТФ в мышцах хватит только на 1 сек работы.
1 этап генерации энергии:
В момент врабатывания мышцы испытывают дефицит
О2, а следовательно, ограничение тканевого дыхания и
окислительного фосфорилирования. Источником АТФ в
момент врабатывания является креатинфосфат.
Это наиболее быстрый путь генерации энергии.
Содержание креатинфосфата в мышцах в 3-8 раза
больше чем АТФ, такое кол-во обеспечивает работу в
течение 3-5 сек.
Источники энергии для мышечного сокращения
Креатинфосфат образуется из креатина и АТФ. Креатин трипептид синтезируется в печени из глицина,аргинина и метионина.
Креатин Р + АДФ
креатин +АТФ
Реакцию катализирует креатинкиназа
Креатинфосфат, неиспользованный, неферментативно
превращается в креатинин
2 этап генерации энергии: включается другой механизм:
Аденилаткиназная реакция: АДФ+АДФ
АТФ+АМФ
3 этап генерации энергии: ускоряется мобилизация
гликогена, ускоряется анаэробный гликолиз, а АМФ
является активатором фосфофруктокиназы
гликолиза. Субстратное фосфорилирование.
4 этап: аэробное окисление углеводов, при длительной
работе жиры. Окислительное фосфорилирование.
Сердечная мышца –аэробна. ВЖК (70%).углеводы,ПК
Креатин, креатинин. Диагностическое значение.
нормаПечень
Гли
Арг
дистрофия мышц
Мышцы
Мышцы
Креатин
креатин
Мет
гли
арг
Креатин Р
Креатинин
моча
Суточное выделение креатинина величина постоянная - прямо
пропорциональная массе.
Креатина в моче нет
Печень
Печень
Мышцы
Мышцы
Креатин
креатин
Креатин Р
мет
Креатин
Креатинин
моча (креатинурия) моча
Креатин не фосфорилируется в мышцах,
уровень в крови повышается. Креатинин в
почках не реабсорбируется,поэтому его
кол-во в моче отражает величину
клубочковой фильтрации.
Функциональная биохимия печени
Печень занимает центральное место в обменевеществ, что определяется своеобразием
топографии и кровоснабжением
Печень – орган – «альтруист». С одной стороны, в
печени синтезируется необходимые вещества для
других органов - белки, фосфолипиды, карнитин,
креатин, кетоновые тела, холестерин, глюкоза. С
другой стороны, обеспечивает защиту органов от
образующихся в них токсических веществ,
чужеродных соединений и микроорганизмов.
Печень выполняет следующие биохимические функции:
1. метаболическую и гомеостатическую;
2. желчеобразовательную и экскреторную
3. депонирующую(депо жирорастворимых витаминов);
4. обезвреживающую - детоксицирующую
Метаболическая и гомеостатическая функция
Выполнение этой функции обусловлено участиемпечени в обмене углеводов, липидов, белков,
пигментном обмене, гемостазе.
Печень обеспечивает синтез и поступление в
кровь необходимых соединений, их
трансформацию, обезвреживание, выведение,
обеспечивая гомеостаз.
Роль печени в углеводном обмене:
В печени глюкоза метаболизируется по всем путямсинтез и мобилизация гликогена, ПФП, глюконеогенез.
Роль печени в углеводном обмене заключается в первую
очередь в обеспечении нормогликемии, за счет
органоспецифичного фермента –
глюкозо-6-фосфатазы.
Роль печени в липидном обмене
Печень участвует во всех этапах обмена липидов, включаяпереваривание и всасывание гидрофобных продуктов
переваривания (желчь-секрет печени).
В абсорбтивный период в печени ускоряется синтез ВЖК,
которые используются для синтеза ТАГ и ФЛ. ФЛ,
синтезируемые в печени (и на экспорт) необходимы всем
тканям, в первую очередь, для построения мембран.
В период голодания – бета-окисление; для окисления
необходим карнитин, который синтезируется в печени.
В период голодания в печени образуются кетоновые тела,
используемые в качестве источника внепеченочными
тканями.
Синтез холестерола, и его перераспределение между
органами за счет образования транспортных форм –
ЛНОНП и ЛПВП. Образование из холестерола желчных
кислот.
Роль печени в белковом обмене.
Около половины белков организма синтезируется в печени как длясобственных нужд, так и секретируемые:
- Белки плазмы крови- глобулины и все альбумины;
- Факторы свертывания – фибриноген и витамин К-зависимые,
факторы системы фибринолиза;
- группа транспортных белков –церуллоплазмин(Сu++)
гаптоглобин, трасферрин, депо железа –ферритин;
- апобелки ЛП;
- белки острой фазы – «С»-реактивный, α1-антитрипсин, α2макроглобулин(при воспалении)
- -креатин.
- синтез заменимых аминокислот;
- небелковые азотистые соединения – азотистые основания,
порфирины, мочевина, мочевая кислота
- В связи с этим активен обмен аминокислот, активны ферменты
трансаминирования – АЛТ и АСТ, дезаминирования –
глутаматдегидрогеназа.
Нарушение белоксинтезирующей функции проявляется
изменением соотношения белков – диспротеинемией.
Участие печени в пигментном обмене – в образовании
глюкуронидов и их экскреции.
Желчеобразовательная и экскреторная функция.
В печени образуются желчные кислоты из холестеролапод действием фермента 7α-холестеролгидроксилазы.
Активность фермента снижается желчными кислотами.
За сутки около 600мг, здесь же первичные кислоты –
холевые и дезоксихолевые конъюгируют с таурином и
гликоколом, образуя тауро- гликохолевые кислоты.
Выведение желчных кислот основной путь выведения
холестерола
Экскреторная функция связана со строением печени. У
каждого гепатоцита одна сторона обращена к желчному
протоку, другая к кровеносному капилляру.
Из печени различные вещества эндо- и экзопроисхождения экскретируются с желчью через
кишечник, или через кровь почками. Нарушение этой
функции сказывается на обмене липидов, накоплении в
организме токсичных продуктов.
Обезвреживающая функция печени.
В организме в процессе жизнедеятельности образуютсятоксичные метаболиты как собственных соединений,
так и чужеродных - ксенобиотиков. Эти соединения могут
быть гидрофильными и гидрофобными.
Примером обезвреживания токсичных продуктов является
синтез мочевины.
Гидрофобные, способны депонироваться в клетках и
неблагоприятно влиять на структуру и метаболизм в
клетке, их необходимо инактивировать.
Печень –уникальный орган, в котором имеются механизмы
обезвреживания (инактивации, детоксикации) таких
соединений. Механизм инактивации таких соединений
построен по общей схеме.
Инактивация может состоять из двух этапов:
модификации и конъюгации.
Этап химической модификации
Этап химической модификации обеспечиваетповышение гидрофильности вещества и обязателен
для всех гидрофобных соединеий.
Повышение гидрофильности обеспечивается
многочисленными реакциями –
гидроксилирования,окисления,
восстановления,гидролиза. В большинстве случаев
этап начинается с реакции гидроксилирования
ферментами мембран гладкого ретикулома клеток –
монооксигеназами. Процесс называется
микросомальным окислением.
Монооксигеназы представлены в виде
электронтранспортной цепи, центральным фермент –
гемпротеид- цитохром Р450 имеет два центра
связывания - с окисляемым веществом и О2. и
обладает широкой субстратной специфичностью.
Источником водорода является НАДФН ПФП
Микросомальное окисление
О22Н+ê
НАДФН+
ФАД(ФМН)редуктаза
ê
ê
цитохром
Р450
Fe+2
2H+
SH
S OH
Fe+3
Н2О
Существует около 1000 изоформ цитохрома с различной специфичностью
Цитохром Р450 один атом кислорода включает в субстрат
(гидроксилирует), другой восстанавливает в воду.
Появление у субстрата гидрофильных свойств обусловливает
возможность 2 этапа инактивации
Этап конъюгации
Коньюгация с с гидрофильными молекулами:УДФ-глюкуроновая кислота,
фосфоаденозинфосфосульфат (ФАФС) и др.
Примеры: образование глюкуронида билирубина,
обезвреживание продуктов гниения белков ЖКТ.
Реакции катализируются трансферазами.
Коньюгация снижает реакционную способность
веществ - их токсичность,повышает
гидрофильность,а значит, выведение из организма.
Не все вещества проходят два эта инактивации.Это
зависит от строения (от степени гидрофильности
токсичного вещества).
Индикаторы нарушений функций печени
При различных заболеваниях печени нарушаются ее функции всеили некоторые. Индикаторами этих нарушений служат изменения
содержания в крови соединений или активность ферментов
поступающих из печени.
Существует ряд тестов, называемых функциональными
печеночными пробами:
Определение активности ферментов АЛТ,АСТ
(коэффициент де Ритисса), Соотношение фракций
белков – на выявление диспротеинемии – осадочные
пробы тимоловая, Вельтмана; Определение
содержания фибриногена; протромбина
Определение билирубина и его видов;
Определение содержания мочевины;
Определение холестерина и соотношение ЛП
Определение активности ферментов гаммаглутамилтранспептидазы; щелочной фосфатазы
(холестаз);
1. Выберите наиболее точный ответ: печень выполняет важную роль в обмене желчных пигментов, которые образуются в результате распада:
2. Цитохромов
3. Витаминов
2. В печени 1/4 часть билирубина связывается с УДФ-глюкуроновой кислотой и называется:
1. Прямой билирубин
2. Диглюкуронид билирубина
3. Непрямой билирубин
4. Гаптоглобин
5. Свободный билирубин
3. Все вещества первичной мочи делят на:
1. Пороговые
2. Беспороговые
3. Проникающие
4. Непроникающие
4. Какими способами трансмембранного транспорта происходит реабсорбция в почках:
1. Простая диффузия
2. Облегченная диффузия
3. Активный транспорт
4. Везикулярный транспорт
5. Укажите неправильное утверждение. В дистальных канальцах почек:
1. Ионы натрия реабсорбируются независимо от воды
2. В обмен на поступающий в эпителий дистальных канальцев натрий в мочу секретируются анионы
3. Реабсорбция ионов натрия регулируется альдостероном
6. Для определения клиренса вводят вещество:
1. Которое фильтруется в клубочках, и не реабсорбируется и не секретируется канальцами нефронов
2. Которое фильтруется в клубочках и реабсорбируется и секретируется канальцами нефронов
3. Которое не фильтруется в клубочках и не реабсорбируется и не секретируется канальцами нефронов
7. При ацидозе количество бикарбонатов в моче:
1. Повышается
2. Снижается
3. Не изменяется
8. Источниками сульфатов мочи являются:
1. Асп, глу
2. Лиз, арг, гис
3. Цис, мет
9. Суточное выделение креатинина зависит от:
1. Характера питания
2. Мышечной массы
3. Интенсивности липолиза
10. В норме креатин в моче присутствует у:
1. Взрослых
3. Стариков
11. Альдостерон:
1. Стимулирует реабсорбцию в почках ионов калия
2. Стимулирует реабсорбцию в почках ионов натрия
12. Повышенное выделение мочевины с мочой наблюдается при:
1. Поражении печени
2. Поражении сердца
3. Голодании, ожогах
13. Глюкозурия наблюдается при повышении содержания глюкозы крови выше:
1. 5, 55 - 6,0 ммоль/л
2. 8,3 - 8,8 ммоль/л
3. 6,1-8,0 ммоль/л
14. Укажите нормальную активность альфа-амилазы в моче
1. 16-30 г/(ч. л.)
2. 28-160 г/(ч. л.)
3. 3,3 - 5,5 ммоль/л
15. Какие камни образуются в кислой моче:
1. Оксалатные
2. Фосфатные
3. Уратные
4. Карбонатные
16. В основе количественного определения белка в моче по методу Робертса-Стольникова -Брандберга лежит:
1. Проба кипячением
2. Проба Геллера
3. Биуретовая реакция
17. Ложная протеинурия наблюдается при патологии:
2. Надпочечников
3. Мочевыводящих путей
18. Ультрафильтрат первичной мочи не содержит белки, молекулярная масса которых выше:
19. Укажите основной источник энергии для работы головного мозга в норме?
1. Кетоновые тела
2. Глюкоза
3. Жирные кислоты
20. Укажите медиаторы ЦНС тормозного типа действия:
3. Глицин
21. Медиатором холинергических синапсов является:
1. Ацетилхолин
2. Фосфатидилхолин
22. Какие аминокислоты преобладают в составе коллагена?
1. Глицин
2. Пролин
3. Аргинин
4. Цистеин
23. Прочность коллагеновых волокон определяется:
24. Соединительная ткань характеризуется наличием:
1. Липопротеинов
2. Протеогликанов
3. Хромопротеинов
25. Прочность коллагеновых волокон определяется:
1. Образованием двойной спирали из полипептидных цепей
2. Образованием тройной спирали из полипептидных цепей
3. Ковалентными связями между молекулами тропоколлагена
4. Гидрофобными взаимодействиями между молекулами тропоколлагена
26. Соединительная ткань характеризуется наличием:
1. Липопротеинов
2. Протеогликанов
3. Хромопротеинов
27. Белок коллаген отличается своим аминокислотным составом. Какие аминокислоты наиболее часто повторяются в полипептидных цепях коллагена?
1. Гли-сер-вал
2. Гли-арг-тир
3. ФГн-гли-цис
4. гли-про-ала
28. Какой компонент соединительной ткани составляет основу рубца?
1. Фибронектин
2. Гликозаминогликаны
3. Коллаген
4. Эластин
29. Какой витамин способствует образованию рубца в заживающей ране?
30. Какой из перечисленных белков осуществляет взаимосвязь клеток, волокон и компонентов основного вещества соединительной ткани в единое целое?
1. Коллаген
2. Эластин
3. Фибронектин
31. Первой фазой биотрансформации ксенобиотиков является:
1. Конъюгация
2. Ферментативная модификация
32. Второй фазой биотрансформации ксенобиотиков является:
1. Конъюгация
2. Ферментативная модификация
3. Стабилизация в липидном бислое мембран
33. Донором ацетильных групп в реакциях конъюгации является:
3. Ацетил-КоА
4. Ацил-КоА
34. Активной формой серной кислоты в реакциях конъюгации является:
1. УДФ-глюкуроновая кислота
2. УДФ-галактоза
35. Источником глюкуроновой кислоты в реакциях конъюгации является:
1. УДФ-глюкуроновая кислота
КУРСОВАЯ РАБОТА:
АНАЛИЗ БИОХИМИЧЕСКИХ ПОКАЗАТЕЛЕЙ РАБОТЫ ПЕЧЕНИ В НОРМЕ И ПАТОЛОГИИ
Cодержание
Введение
1.1.2 Регуляция липидного обмена
1.1.3 Регуляция обмена белков
1.2 Мочевинообразовательная функция
1.3 Желчеобразовательная и экскреторная функция
1.4 Биотрансформационная (обезвреживающая) функция
2. Заболевания печени и лабораторная диагностика заболеваний печени
2.1 Основы клинической лабораторной диагностики заболеваний печени
2.2 Основные клинико-лабораторные синдромы при поражениях печени
2.2.1 Синдром цитолиза
2.2.4 Синдром воспаления
2.2.5 Синдром шунтирования печени
Заключение
Биохимия печени включает как протекание нормальных обменных процессов, так и нарушения метаболизма веществ с развитием патологии. Изучение всех аспектов биохимии печени позволит видеть картину нормально функционирующего органа и его участие в работе всего организма и поддержании гомеостаза. Так же при нормальной работе печени осуществляется интеграция всех основных обменов в организме, причем удается наблюдать начальные этапы метаболизма (например, при первичном всасывании веществ из кишечника) и конечные этапы с последующим выведением продуктов обмена из организма.
При нарушениях работы печени происходит сдвиг метаболизма в определенную сторону, поэтому необходимо изучение патологических состояний органа для дальнейшей диагностики заболеваний. В настоящее время это особенно актуально, так как заболевания печени прогрессируют, а достаточно хороших методов лечения пока не существует. К таким заболеваниям в первую очередь относятся вирусные гепатиты, циррозы печени (часто при систематическом употреблении алкоголя и при прочих вредных внешних воздействиях, связанных с неблагоприятной экологией), сдвиги метаболизма при нерациональном питании, онкологические заболевания печени. Поэтому очень важна ранняя диагностика этих заболеваний, которая может основываться на биохимических показателях.
Целью курсовой работы является рассмотрение функций печени и сравнение биохимических показателей работы этого органа в норме и патологии; также указание основных принципов лабораторной диагностики, краткое описание синдромов гепатитов различной этиологии и приведение примеров.
1. Функциональная биохимия печени
Условно функции печени по биохимическим показателям можно разделить на: регуляторно-гомеостатическую функцию, включающую основные виды обмена (углеводный, липидный, белковый, обмен витаминов, водно-минеральный и пигментный обмены), мочевинообразовательную, желчеобразовательную и обезвреживающую функции. Такие основные функции и их регуляция подробно рассмотрены далее в этой главе.
1.1 Регуляторно-гомеостатическая функция печени
Печень - центральный орган химического гомеостаза, где чрезвычайно интенсивно протекают все обменные процессы и где они тесно переплетаются между собой.
1.1.1 Углеводный обмен в печени и его регуляция
Моносахариды (в частности глюкоза) поступают в печень по воротной вене и подвергаются различным преобразованиям. Например, при избыточном поступлении глюкозы из кишечника она депонируется в виде гликогена, так же глюкоза производится печенью в ходе гликогенолиза и глюконеогенеза, поступает в кровь и расходуется большинством тканей. Регуляция углеводного обмена осуществляется благодаря тому, что печень является практически единственным органом, который поддерживает постоянный уровень глюкозы в крови даже в условиях голодания.
Судьба моносахаридов различна в зависимости от природы, их содержания в общем кровотоке, потребностей организма. Часть их отправится в печёночную вену, чтобы поддержать гомеостаз, в первую очередь, глюкозы крови и обеспечить нужды органов. Концентрация глюкозы в крови определяется балансом скоростей ее поступления, с одной стороны, и потребления тканями с другой. В постабсорбтивном состоянии (постабсорбтивное состояние развивается через 1,5—2 часа после приема пищи, так же называется истинным или метаболическим насыщением . Типичным постабсорбтивным состоянием считают состояние утром до завтрака, после примерно десятичасового ночного перерыва в приеме пищи) и в норме концентрация глюкозы в крови равна 60-100 мг/дл (3,3-5,5 мольл). А остальную часть моносахаридов (в основном глюкозы) печень использует для собственных нужд.
В гепатоцитах интенсивно протекает метаболизм глюкозы. Поступившая с пищей глюкоза только в печени с помощью специфических ферментных систем преобразуются в глюкозо-6-фосфат (лишь в такой форме глюкоза используется клетками) . Фосфорилирование свободных моносахаридов - обязательная реакция на пути их использования, она приводит к образованию более реакционно-способных соединений и поэтому может рассматриваться как реакция активации. Галактоза и фруктоза, поступающие из кишечного тракта, при участии соответственно галактокиназы и фруктокиназы фосфорилируются по первому углеродному атому:
Глюкоза, поступающая в клетки печени, так же подвергается фосфорилированию с использованием АТФ. Эту реакцию катализирует ферменты гексокиназа и глюкокиназа.
печень патология диагностика заболевание
Гексокиназа обладает высоким сродством к глюкозе (К м
Наряду с другими механизмами это предотвращает черезмерное повышение концентрации глюкозы в периферической крови при пищеварении .
Образование глюкозо-6-фосфата в клетке - своеобразная «ловушка» для глюкозы, так как мембрана клетки непроницаема для фосфорилированной глюкозы (нет соответствующих транспортных белков). Кроме того, фосфорилирование уменьшает концентрацию свободной глюкозы в цитоплазме. В результате создаются благоприятные условия для облегченной диффузии глюкозы в клетки печени из крови.
Возможна и обратная реакция превращения глюкозо-6-фосфат в глюкозу при действии глюкозо-6-фосфатазы, которая катализирует отщепление фосфатной группы гидролитическим путем.
Образовавшаяся свободная глюкоза способна диффундировать из печени в кровь. В других органах и тканях (кроме почек и клеток кишечного эпителия) глюкозо-6-фосфатазы нет, и поэтому там проходит только фосфорилирование, без обратной реакции, и выход глюкозы из этих клеток невозможен .
Глюкозо-6-фосфат может превратиться в глюкозо-1-фосфат при участии фосфоглюкомутазы, которая катализирует обратимую реакцию.
Так же глюкозо-6-фосфат может использоваться в различных превращениях, основными из которых являются: синтез гликогена, катаболизм с образованием СО 2 и Н 2 О или лактата, синтез пентоз. Вместе с тем в процессе метаболизма глюкозо-6-фосфата образуются промежуточные продукты, используемые в дальнейшем для синтеза аминокислот, нуклеотидов, глицерина и жирных кислот. Таким образом, глюкозо-6-фосфат - не только субстрат для окисления, но и строительный материал для синтеза новых соединений (приложение 1).
Итак, рассмотрим окисление глюкозы и глюкозо-6-фосфата в печени. Этот процесс идет двумя путями: дихотомическим и апотомическим. Дихотомический путь это гликолиз, который включает «анаэробный гликолиз», завершающийся образованием молочной кислоты (лактата) или этанола и СО 2 и «аэробный гликолиз» - распад глюкозы, проходящий через образование глюкозо-6-фосфата, фруктозобисфосфата и пирувата как в отсутствие так и в присутствие кислорода (аэробный метаболизм пирувата выходит за рамки углеводного обмена, однако может рассматриваться как завершающая его стадия: окисление продукта гликолиза - пирувата).
Апотомический путь окисления глюкозы или пентозный цикл заключается в образовании пентоз и возвращению пентоз в гексозы в результате распадается одна молекула глюкозы и образуется СО 2 .
Гликолиз в анаэробных условиях - сложный ферментативный процесс распада глюкозы, протекающий без потребления кислорода. Конечным продуктом гликолиза является молочная кислота. В процессе гликолиза образуется АТФ.
Процесс гликолиза протекает в гиалоплазме (цитозоле) клетки и условно делится на одиннадцать этапов, которые соответственно катализируют одиннадцать ферментов:
- Фосфорилирование глюкозы и образование глюкозо-6-фосфата - перенос остатка ортофосфата на глюкозу за счет энергии АТФ. Катализатором является гексокиназа. Этот процесс был рассмотрен выше.
- Превращение глюкозо-6-фосфата под действием фермента глюкозо-6-фосфат-изомеразы во фруктозо-6-фосфат:
- Фруктозо-6-фосфат вновь фосфорилируется за счет второй молекулы АТФ, реакция катализируется фосфофруктокиназой:
Реакция необратима, протекает в присутствии ионов магния и является наиболее медленно текущей реакцией гликолиза.
- Под влиянием фермента альдолазы фруктозо-1,6-бифосфат расщепляется на две фосфотриозы:
- Реакция изомеризации триозофосфатов. Катализируеися ферментом триозофосфатизомеразой:
- Глицеральдегид-3-фосфат в присутствии фермента глицеральдегидфосфатдегидрогеназы, кофермента НАД и неорганического фосфата продвергается своеобразному окислению с образованием 1,3-бифосфоглицериновой кислоты и восстановленой формы НАД - НАД*Н 2:
- Реакция катализируется фосфоглицераткиназой, происходит передача фосфатной группы в положении 1 на АДФ с образованием АТФ и 3-фосфоглицериновой кислоты (3-фосфоглицерат):
- Внутримолекулярный перенос оставшейся фосфатной группы, и 3-фосфоглицериновая кислота превращается в 2-фосфорлицериновую кислоту (2-фосфоглицерат):
Реакция легкообратима и протекает в присутствии ионов магния.
9. Реакция катализируется ферментом енолазой, 2-фосфоглицериновая кислота в результате отщепления молекулы воды переходит в фосфоенолпировиноградную кислоту (фосфоенолпируват), а фосфатная связь в положении 2 становится макроэргической:
- Разрыв макроэргической связи и перенос фосфатного остатка от фосфоенолпирувата на АДФ. Кртализируется ферментом пируваткиназой:
11. Восстановление пировиноградной кислоты и образование молочной кислоты (лактата). Реакция протекает при участии фермента лактатдегидрогеназы и кофермента НАД*Н 2, образовавшегося в шестой ркакции:
Гликолиз в аэробных условиях . В этом процессе можно выделить три части:
1. специфические для глюкозы превращения, завершающиеся образованием пирувата (аэробный гликолиз);
2. общий путь катаболизма (окислительное декарбоксилирование пирувата и цитратный цикл);
3. митохондриальная цепь переноса электронов.
В результате этих процессов глюкоза в печени распадается до С0 2 и Н 2 0, а освобождающаяся энергия используется для синтеза АТФ (приложение 2).
К обмену углеводов в печени относятся только специфические для глюкозы превращения, где происходит распад глюкозы до пирувата, который можно разделить на два этапа:
1. От глюкозы до глицеральдегидфосфата. В реакциях происходит включение фосфатных остатков в гексозы и превращение гексозы в триозу (приложение 3). Реакции этого этапа катализируют следующие ферменты: гексокиназа или глюкокиназа (1); фосфоглюкоизомераза (2); фосфофруктокиназа (3); альдолаза фруктозо-1,6-бисфосфата (4); фосфотриозоизомераза (5)
2. От глицеральдегидфосфата до пирувата. Это реакции, связанные с синтезом АТФ. Этап завершается превращением каждой молекулы глюкозы в две молекулы глицеральдегидфосфата (приложение 4). В реакциях участвуют пять ферментов: дегидрогеназа глицеральдегидфосфата (6); фосфоглицераткиназа (7); фосфоглицеромутаза (8); енолаза (9); пируваткиназа (10).
Пентозофосфатный (фосфоглюконатный) путь превращения глюкозы обеспечивает клетку гидрированным НАДФ для восстановительных синтезов и пентозами для синтеза нуклеотидов. В пентозофосфатном пути можно выделить две части — окислительный и неокислительный пути.
- Окислительный путь включает две реакции дегидрирования, где акцептором водорода служит НАДФ (приложение 5). Во второй реакции одновременно происходит декарбоксилирование, углеродная цепь укорачивается на один атом углерода и получаются пентозы.
- Неокислительный путь значительно сложнее. Здесь нет реакций дегидрирования, он может служить только для полного распада пентоз (до С0 2 и Н 2 0) или для превращения пентоз в глюкозу (приложение 6). Исходными веществами являются пять молекул фруктозо-6-фосфата, в сумме содержащие 30 углеродных атомов, конечный продукт реакции — шесть молекул рибозо-5-фосфата, в сумме также содержащие 30 углеродных атомов.
Окислительный путь образования пентоз и путь возращения пентоз в гексозы вместе составляют циклический процесс:
В этом цикле за один оборот полностью распадается одна молекула глюкозы, все шесть углеродных атомов которой превращаются в С0 2 .
Так же в печени идет обратный гликолизу процесс - глюконеогенез. Глюконеогенез — процесс синтеза глюкозы из веществ неуглеводной природы. Его основной функцией является поддержание уровня глюкозы в крови в период длительного голодания и интенсивных физических нагрузок. Глюконеогенез обеспечивает синтез 80-100 г глюкозы в сутки. Первичные субстраты глюконеогенеза — лактат, аминокислоты и глицерол. Включение этих субстратов в глюконеогенез зависит от физиологического состояния организма. Лактат — продукт анаэробного гликолиза. Он образуется при любых состояниях организма в эритроцитах и работающих мышцах. Таким образом, лактат используется в глюконеогенезе постоянно. Глицерол высвобождается при гидролизе жиров в жировой ткани в период голодания или при длительной физической нагрузке. Аминокислоты образуются в результате распада мышечных белков и включаются в глюконеогенез при длительном голодании или продолжительной мышечной работе. Необходимо отметить, что гликолиз протекает в цитозоле, а часть реакций глюконеогенеза происходит в митохондриях .
Глюконеогенез в основном протекает по тому же пути, что и гликолиз, но в обратном направлении (приложение 7). Однако три реакции гликолиза необратимы, и на этих стадиях реакции глюконеогенеза отличаются от реакций гликолиза.
Превращение пирувата в фосфоенолпируват (необратимая стадия I) осуществляется при участии двух ферментов: пируваткарбоксилазы и карбоксикиназы фосфоенолпирувата:
Две другие необратимые стадии катализируются фосфатазой фруктозо-1,6-бисфосфата и фосфатазой глюкозо-6-фосфата:
Каждая из необратимых реакций гликолиза вместе с соответствующей ей реакцией глюконеогенеза образует субстратный цикл (приложение 7, реакции 1, 2, 3).
Синтез глюкозы (глюконеогенез из аминокислот и глицерина) . Глюкоза в печени может синтезироваться из аминокислот и глицерина. При катаболизме аминокислот в качестве промежуточных продуктов образуются пируват или оксалоацетат, которые могут включаться в путь глюконеогенеза на стадии первого субстратного цикла (приложение 7, реакция 1). Глицерин образуется при гидролизе жиров и может превращаться в глюкозу (приложение 8). Аминокислоты и глицерин используются для синтеза глюкозы главным образом при голодании или при низком содержании углеводов в рационе (углеводное голодание).
Глюконеогенез может так же происходить из лактата. Молочная кислота не является конечным продуктом обмена, но ее образование — это тупиковый путь метаболизма: единственный способ использования молочной кислоты связан с ее превращением вновь в пируват при участии той же лактатдегидрогеназы:
Из клеток, в которых происходит гликолиз, образующаяся молочная кислота поступает в кровь и улавливается в основном печенью, где и превращается в пируват. Пируват в печени частично окисляется, частично превращается в глюкозу — цикл Кори, или глюкозолактатпый цикл:
В организме взрослого человека за сутки может синтезироваться около 80 г глюкозы, главным образом в печени. Биологическое значение глюконеогенеза заключается не только в возвращении лактата в метаболический фонд углеводов, но и в обеспечении глюкозой мозга при недостатке углеводов в организме, например, при углеводном или полном голодании .
Синтез гликогена (гликогенез) . Как уже говорилось выше, часть глюкозы поступившей в печень используется в синтезе гликогена. Гликоген — разветвленный гомополимер глюкозы, в котором остатки глюкозы соединены в линейных участках a-1,4-гликозидной связью. В точках ветвления мономеры соединены a-1,6-гликозидными связями. Эти связи образуются примерно с каждым десятым остатком глюкозы. Так возникает древообразная структура с молекулярной массой >10 7 Д, что соответствует приблизительно 50 000 остатков глюкозы (приложение 9). При полимеризации глюкозы снижается растворимость образующейся молекулы гликогена и, следовательно, ее влияние на осмотическое давление в клетке. Это обстоятельство объясняет, почему в клетке депонируется гликоген, а не свободная глюкоза.
Гликоген хранится в цитозоле клетки в форме гранул диаметром 10—40 нм. После приёма пищи, богатой углеводами, запас гликогена в печени может составлять примерно 5% от её массы.
Распад гликогена печени служит в основном для поддержания уровня глюкозы в крови в постабсорбтивном периоде. Поэтому содержание гликогена в печени изменяется в зависимости от ритма питания. При длительном голодании оно снижается почти до нуля.
Гликоген синтезируется в период пищеварения (через 1—2 ч после приёма углеводной пищи). Синтез гликогена из глюкозы требует затрат энергии.
Прежде всего глюкоза подвергается фосфорилированию при участии фермента гексокиназы и глюкокиназы. Далее глюкозо-6-фосфат под влиянием фермента фосфоглюкомутазы переходит в глюкозо-1-фосфат.
Образовавшийся глюкозо-1-фосфат уже непосредственно вовлекается в синтез гликогена.
На первой стадии синтеза глюкозо-1-фосфат вступает во взаимодействие с УТФ (уридинтрифосфат), образуя уридиндифосфатглюкозу (УДФ-глюкоза) и пирофосфат. Данная реакция катализируется ферментом глюкозо-1-фосфат-уридилилтрансферазой (УДФГ-пирофосфорилаза) (приложение 10).
На второй стадии — стадии образования гликогена — происходит перенос глюкозного остатка, входящего в состав УДФ-глюкозы, на глюкозидную цепь гликогена («затравочное» количество) (приложение 11). При этом образуется б-1,4-гликозидная связь между первым атомом углерода добавляемого остатка глюкозы и 4-гидроксильной группой остатка глюкозы цепи. Эта реакция катализируется ферментом гликогенсинтазой. Образующийся УДФ затем вновь фосфорилируется в УТФ за счет АТФ, и таким образом весь цикл превращений глюкозо-1-фосфата начинается сначала.
Установлено, что гликогенсинтаза неспособна катализировать образование б-1,6-гликозидную связь, имеющуюся в точках ветвления гликогена. Этот процесс катализирует специальный фермент, получивший название гликогенветвящего фермента, или амило-1,4-1,6-трансглюкозидазы. Последний катализирует перенос концевого олигосахаридного фрагмента, состоящего из 6 или 7 остатков глюкозы, с нередуцирующего конца одной из боковых цепей, насчитывающей не менее 11 остатков, на 6-гидроксиль-ную группу остатка глюкозы той же или другой цепи гликогена. В результате образуется новая боковая цепь. Ветвление увеличивает скорость синтеза и расщепления гликогена .
Распад гликогена или его мобилизация происходят в ответ на повышение потребности организма в глюкозе. Гликоген печени распадается в основном в интервалах между приёмами пищи, распад ускоряется во время физической работы. Распад гликогена происходит при участии двух ферментов: гликогенфосфорилазы и фермента с двойной специфичностью — 4:4-трансферазы-б-1,6-гликозидазы. Гликогенфосфорилаза катализирует фосфоролиз 1,4-гликозидной связи нередуцирующих концов гликогена, глюкозные остатки отщепляются один за другим в форме глюкозо-1-фосфата (приложение 12). При этом гликогенфосфорилаза не может отщеплять глюкозные остатки от коротких ветвей, содержащих менее пяти глюкозных остатков; такие ветви удаляются 4:4-трансферазой-б-1,6-гликозидазой. Этот фермент катализирует перенос фрагмента из трех остатков короткой ветви на концевой глюкозный остаток более длинной ветви; кроме того, он гидролизует 1,6-гликозидную связь и таким образом удаляет последний остаток ветви (приложение 13).
Голодание в течение 24 ч приводит практически к полному исчезновению гликогена в клетках печени. Однако при ритмичном питании каждая молекула гликогена может существовать неопределенно долго: при отсутствии пищеварения и поступления в ткани глюкозы молекулы гликогена уменьшаются за счет расщепления периферических ветвей, а после очередного приема пищи вновь вырастают до прежних размеров.
Глюкозо-1-фосфат, образующийся из гликогена, при участии фосфоглюкомутазы превращается в глюкозо-6-фосфат, дальнейшая судьба которого в печени и в мышцах различна. В печени глюкозо-6-фосфат превращается в глюкозу при участии глюкозо-6-фосфатазы, глюкоза выходит в кровь и используется в других органах и тканях.
Регуляция процессов гликогенеза и гликогенолиза осуществляется гормонами: инсулином, глюкагоном, адреналином. Первичный сигнал для синтеза инсулина и глюкагона — изменение концентрации глюкозы в крови. Инсулин и глюкагон постоянно присутствуют в крови, но при смене абсорбтивного периода на постабсорбтивный изменяется их относительная концентрация, что является главным фактором, переключающим метаболизм гликогена в печени. Отношение концентрации инсулина в крови к концентрации глюкагона называют «инсулин-глюкагоновый индекс». В постабсорбтивном периоде инсулин-глюкагоновый индекс снижается, и решающее значение в регуляции концентрации глюкозы и крови приобретает концентрация глюкагона. В период пищеварения преобладает влияние инсулина, так как инсулин-глюкагоновый индекс в этом случае повышается. В целом инсулин влияет на обмен гликогена противоположно глюкагону. Инсулин снижает концентрацию глюкозы в крови в период пищеварения.
Гормон адреналин стимулирует выведение глюкозы из печени в кровь, для того чтобы снабдить ткани (в основном мозг и мышцы) «топливом» в экстремальной ситуации.
Регуляторным фактором в метаболизме гликогена является также величина К м глюкокиназы, которая много выше, чем К м гексокиназы - печень не должна потреблять глюкозу для синтеза гликогена, если её количество в крови в пределах нормы.
Липидный обмен в печени включает биосинтез различных липидов (холестерина, триацилглицерина, фосфоглицеридов, сфингомиелина и др.) которые поступают в кровь и распределяются по другим тканям и сгорание (окисление) жирных кислот с образованием кетоновых тел, которые используются как источник энергии для внепеченочных тканей.
Доставка жирных кислот к месту окисления - к митохондриям клеток печени - происходит сложным путем: при участии альбумина осуществляется транспорт жирных кислот в клетку; при участии специальных белков - транспорт в пределах цитозоля; при участии карнитина - транспорт жирной кислоты из цитозоля в митохондрии.
Процесс окисления жирных кислот складывается из следующих основных этапов.
- Активация жирных кислот. Активация протекает на наружной поверхности мембраны митохондрии при участии АТФ, коэнзима А (HS-KoA) и ионов Mg 2+ . Реакция катализируется ферментом ацил-КоА-синтетазой:
Активация протекает в 2 этапа. Сначала жирная кислота реагирует с АТФ с образованием ациладенилата, далее сульфгидрильная группа КоА действует на прочно связанный с ферментом ациладенилат с образованием ацил-КоА и АМФ.
Затем следует транспорт жирных кислот внутрь митохондрий. Переносчиком активированных жирных кислот с длинной цепью через внутреннюю митохондриальную мембрану служит карнитин. Ацильная группа переносится с атома серы КоА на гидроксильную группу карнитина.
2. Образуется ацилкарнитин, который диффундирует через внутреннюю митохондриальную мембрану:
Реакция протекает при участии спецефического цитоплазматического фермента карнитин-ацилтрансферазы. После прохождения ацилкарнитина через мембрану митохондрий происходит обратная реакция - расщепление ацилкарнитина при участии HS-KoA и митохондриальной карнитин-ацилтрансферазы:
3. Внутримитохондриальное окисление жирных кислот. Процесс окисления жирной кислоты в митохондриях клетки включает несколько последовательных реакций.
Первая стадия дегидрирования. Ацил-КоА в митохондриях подвергается ферментативному дегидрированию, при этом ацил-КоА теряет 2 атома водорода в б- и в-положениях, превращаясь в КоА-эфир ненасыщенной кислоты. Реакцию катализирует ацил-КоА-дегидрогеназа, продуктом является еноил-КоА:
Стадия гидратации. Ненасыщенный ацил-КоА (еноил-КоА) при участии фермента еноил-КоА-гидратазы присоединяет молекулу воды. В результате образуется в-оксиацил-КоА (или 3-гидроксиацил-КоА):
Вторая стадия дегидрирования. Образовавшийся в-оксиацил-КоА (3-гидроксиацил-КоА) затем дегидрируется. Эту реакцию катализируют НАД-зависимые дегидрогеназы:
Тиолазная реакция. Расщепление 3-оксоацил-КоА с помощью тиоловой группы второй молекулы КоА. В результате образуется укороченный на два углеродных атома ацил-КоА и двууглеродный фрагмент в виде ацетил-КоА. Данная реакция катализируется ацетил-КоА-ацилтрансферазой (в-ке-тотиолазой):
Образовавшийся ацетил-КоА подвергается окислению в цикле трикарбоновых кислот, а ацил-КоА, укоротившийся на два углеродных атома, снова многократно проходит весь путь в-окисления вплоть до образования бутирил-КоА (4-углеродное соединение), который в свою очередь окисляется до 2 молекул ацетил-КоА .
Биосинтез жирных кислот . Синтез жирных кислот протекает в цитоплазме клетки. В митохондриях в основном происходит удлинение существующих цепей жирных кислот. Установлено, что в цитоплазме печеночных клеток синтезируется пальмитиновая кислота (16 углеродных атомов), а в митохондриях этих клеток из этой пальмитиновой кислоты или из жирных кислот экзогенного происхождения, т.е. поступающих из кишечника, образуются жирные кислоты, содержащие 18, 20 и 22 углеродных атома.
Митохондриальная система биосинтеза жирных кислот, включает несколько модифицированную последовательность реакций в-окисления, и осуществляет только удлинение существующих в организме среднецепочечных жирных кислот, в то время как полный биосинтез пальмитиновой кислоты из ацетил-КоА активно протекает в цитозоле, т.е. вне митохондрий, по совершенно другому пути.
Внемитохондриальная система биосинтеза жирных кислот (липогенез) находится в растворимой (цитозольной) фракции клеток печени. Биосинтез жирных кислот протекает с участием НАДФН, АТФ, Мn2+ и НСО3- (в качестве источника СО2); субстратом является ацетил-КоА, конечным продуктом - пальмитиновая кислота.
Образование ненасыщенных жирных кислот . Элонгация жирных кислот .
Две наиболее распространенные мононенасыщенные жирные кислоты - пальмитоолеиновая и олеиновая - синтезируются из пальмитиновой и стеариновой кислот. Эти превращения протекают в микросомах клеток печени. Превращению подвергаются только активированные формы пальмитиновой и стеариновой кислот. Ферменты, участвующие в этих превращениях, получили название десатураз. Наряду с десатурацией жирных кислот (образование двойных связей) в микросомах происходит и их удлинение (элонгация), причем оба эти процесса могут сочетаться и повторяться. Удлинение цепи жирной кислоты происходит путем последовательного присоединения к соответствующему ацил-КоА двууглеродных фрагментов при участии малонил-КоА и НАДФН. Ферментная система, катализирующая удлинение жирных кислот, получила название элонгазы. Пути превращения пальмитиновой кислоты в реакциях десатурации и элонгации представлены в приложении 14.
Биосинтез триглицеридов . Синтез триглицеридов происходит из глицерина и жирных кислот (главным образом стеариновой, пальмитиновой и олеиновой). Первый путь биосинтеза триглицеридов в печени протекает через образование б-глицерофосфата (глицерол-3-фосфата) как промежуточного соединения, глицерин фосфорилируется за счет АТФ с образованием глицерол-3-фосфата:
Второй путь в основном связан с процессами гликолиза и гликогенолиза. Известно, что в процессе гликолитического распада глюкозы образуется дигидроксиацетонфосфат, который в присутствии цитоплазматической глицерол-3-фосфатдегидрогеназы способен превращаться в глицерол-3-фосфат:
Образовавшийся тем или иным путем глицерол-3-фосфат последовательно ацилируется двумя молекулами КоА-производного жирной кислоты. В результате образуется фосфатидная кислота (фосфатидат):
Ацилирование глицерол-3-фосфата протекает последовательно, т.е. в 2 этапа. Сначала глицерол-3-фосфат-ацилтрансфераза катализирует образование лизофосфатидата. Далее фосфатидная кислота гидролизуется фосфатидат-фосфогидролазой до 1,2-диглицерида (1,2-диацилглицерола):
Затем 1,2-диглицерид ацилируется третьей молекулой ацил-КоА и превращается в триглицерид (триацилглицерол). Эта реакция катализируется диацилглицерол-ацилтрансферазой:
Установлено, что большинство ферментов, участвующих в биосинтезе триглицеридов, находятся в эндоплазматическом ретикулуме, и только некоторые, например глицерол-3-фосфат-ацилтрансфераза,- в митохондриях.
Метаболизм фосфолипидов . Фосфолипиды играют важную роль в структуре и функции клеточных мембран, активации мембранных и лизосомальных ферментов, в проведении нервных импульсов, свертывании крови, иммунологических реакциях, процессах клеточной пролиферации и регенерации тканей, в переносе электронов в цепи дыхательных ферментов. Особая роль фосфолипидам отводится в формировании липопротеидных комплексов. Наиболее важные фосфолипиды синтезируются главным образом в эндоплазматической сети клетки.
Центральную роль в биосинтезе фосфолипидов играют 1,2-диглицериды (в синтезе фосфатидилхолинов и фосфатидилэтаноламинов), фосфатидная кислота (в синтезе фосфатидилинозитов) и сфингозин (в синтезе сфингомиелинов). Цитидинтрифосфат (ЦТФ) участвует в синтезе практически всех фосфолипидов.
Биосинтез холестерина . В синтезе холестерина можно выделить три основные стадии: I - превращение активного ацетата в мевалоновую кислоту, II - образование сквалена из мевалоновой кислоты, III - циклизация сквалена в холестерин.
Рассмотрим стадию превращения активного ацетата в мевалоновую кислоту. Начальным этапом синтеза мевалоновой кислоты из ацетил-КоА является образование ацетоацетил-КоА посредством обратимой тиолазной реакции. Затем при последующей конденсации ацетоацетил-КоА с 3-й молекулой ацетил-КоА при участии гидроксиметилглутарил-КоА-синтазы (ГМГ-КоА-синтаза) образуется в-гидрокси-в-метилглутарил-КоА. Далее в-гидрокси-в-метилглутарил-КоА под действием регуляторного фермента НАДФ-зависимой гидроксиметилглутарил-КоА-редуктазы (ГМГ-КоА-редуктаза) в результате восстановления одной из карбоксильных групп и отщепления HS-KoA превращается в мевалоновую кислоту.
Наряду с классическим путем биосинтеза мевалоновой кислоты имеется второй путь, в котором в качестве промежуточного субстрата образуется в-гидрокси-в-метилглутарил-S-АПБ. Реакции этого пути идентичны начальным стадиям биосинтеза жирных кислот вплоть до образования ацетоацетил-S-АПБ. В образовании мевалоновой кислоты по этому пути принимает участие ацетил-КоА-карбоксилаза - фермент, осуществляющий превращение ацетил-КоА в малонил-КоА.
На II стадии синтеза холестерина мевалоновая кислота превращается в сквален. Реакции II стадии начинаются с фосфорилирования мевалоновой кислоты с помощью АТФ. В результате образуется 5-фосфорный эфир, а затем 5-пирофосфорный эфир мевалоновой кислоты 5-пирофосфомевалоновая кислота в результате последующего фосфорилирования третичной гидроксильной группы образует нестабильный промежуточный продукт - 3-фосфо-5-пирофосфомевалоновую кислоту, которая, декарбоксилируясь и теряя остаток фосфорной кислоты, превращается в изопентенилпирофосфат. Последний изомеризуется в диметил-аллилпирофосфат. Затем оба изомерных изопентенилпирофосфата (диметилаллилпирофосфат и изопентенилпирофосфат) конденсируются с высвобождением пирофосфата и образованием геранилпирофосфата. К геранилпирофосфату вновь присоединяется изопентенилпирофосфат. В результате этой реакции образуется фарнезилпирофосфат. В заключительной реакции данной стадии в результате НАДФН-зависимой восстановительной конденсации 2 молекул фарнезилпирофосфата образуется сквален.
На III стадии биосинтеза холестерина сквален под влиянием сквален-оксидоциклазы циклизируется с образованием ланостерина. Дальнейший процесс превращения ланостерина в холестерин включает ряд реакций, сопровождающихся удалением трех метильных групп, насыщением двойной связи в боковой цепи и перемещением двойной связи.
Общая схема синтеза холестерина представлена в приложении 15.
Метаболизм кетоновых тел . Под термином кетоновые (ацетоновые) тела подразумевают ацетоуксусную кислоту (ацетоацетат) СН3СОСН2СООН, в-оксимасляную кислоту (в-оксибутират, или D-3-гидроксибутират) СН3СНОНСН2СООН и ацетон СН3СОСН3.
Образование кетоновых тел происходит в несколько этапов (приложение 16). На первом этапе из 2 молекул ацетил-КоА образуется ацетоацетил-КоА. Реакция катализируется ферментом ацетил-КоА-ацетилтрансферазой (3-кетотиолазой). Затем ацетоацетил-КоА взаимодействует еще с одной молекулой ацетил-КоА. Реакция протекает под влиянием фермента гидроксиметилглутарил-КоА-синтетазы. Образовавшийся в-окси-в-метилглутарил-КоА способен под действием гидроксиметилглутарил-КоА-лиазы расщепляться на ацетоацетат и ацетил-КоА. Ацетоацетат восстанавливается при участии НАД-зависимой D-3-гидроксибутиратдегидрогеназы, при этом образуется D-в-оксимасляная кислота (D-3-гидроксибутират).
Существует второй путь синтеза кетоновых тел. Образовавшийся путем конденсации 2 молекул ацетил-КоА ацетоацетил-КоА способен отщеплять коэнзим А и превращаться в ацетоацетат. Этот процесс катализируется ферментом ацетоацетил-КоА-гидролазой (деацилазой). Однако второй путь образования ацетоуксусной кислоты (ацетоацетата) не имеет существенного значения, так как активность деацилазы в печени низкая.
В крови здорового человека кетоновые тела содержатся лишь в очень небольших концентрациях (в сыворотке крови 0,03-0,2 ммоль/л). Следует подчеркнуть важную роль кетоновых тел в поддержании энергетического баланса. Кетоновые тела - поставщики топлива для мышц, почек и действуют, возможно, как часть регуляторного механизма с обратной связью, предотвращая чрезвычайную мобилизацию жирных кислот из жировых депо. Печень в этом смысле является исключением, она не использует кетоновые тела в качестве энергетического материала. Из митохондрий печени эти соединения диффундируют в кровь и переносятся к периферическим тканям.
Печень является центральным местом обмена ВЖК. Сюда они поступают из кишечника, жировых депо в составе альбуминов плазмы крови .
Регуляция синтеза и распада жиров в печени . В клетках печени есть активные ферментные системы и синтеза, и распада жиров. Регуляция обмена жиров в значительной мере определяется регуляцией обмена жирных кислот, но не исчерпывается этими механизмами. Синтез жирных кислот и жиров активируется при пищеварении, а их распад — в постабсорбтивном состоянии и при голодании. Кроме того, скорость использования жиров пропорциональна интенсивности мышечной работы. Регуляция обмена жиров тесно сопряжена с регуляцией обмена глюкозы. Как и в случае обмена глюкозы, в регуляции обмена жиров важную роль играют гормоны инсулин, глюкагон, адреналин и процессы переключения фосфорилирования-дефосфорилирования белков.
Регуляция обмена белков в печени осуществляется благодаря интенсивному биосинтезу в ней белков и окислению аминокислот. За сутки в организме человека образуется около 80—100 г белка, из них половина в печени. При голодании печень быстрее всех расходует свои резервные белки для снабжения аминокислотами других тканей. Потери белка в печени составляют примерно 20%; в то время как в других органах не более 4%. Белки самой печени в норме обновляются полностью каждые 20 суток. Большинство синтезированных белков печень отправляет в плазму крови. При потребности (например, при полном или белковом голодании) эти протеины так же служат источниками необходимых аминокислот.
Поступив через воротную вену в печень, аминокислоты подвергаются ряду превращений, так же значительная часть аминокислот разносится кровью по всему организму и используется для физиологических целей. Печень обеспечивает баланс свободных аминокислот организма путем синтеза заменимых аминокислот и перераспределения азота. Всосавшиеся аминокислоты в первую очередь используются в качестве строительного материала для синтеза специфических тканевых белков, ферментов, гормонов и других биологически активных соединений. Некоторое количество аминокислот подвергается распаду с образованием конечных продуктов белкового обмена (СО2, Н2О и NH3) и освобождением энергии.
Все альбумины, 75-90% б-глобулинов (б 1 -антитрипсин, б 2 -макроглобулин - ингибиторы протеаз, белки острой фазы воспаления), 50% в-глобулинов плазмы синтезируются гепатоцитами. В печени происходит синтез белковых факторов свертывания крови (протромбина, фибриногена, проконвертина, акцелератора глобулина, фактора Кристмаса, фактора Стюарта-Прауэра) и часть естественных основных антикоагулянтов (антитромбин, протеин С и др.). Гепатоциты участвуют в образовании некоторых ингибиторов фибринолиза, регуляторы эритропоэза - эритропоэтины - образуются в печени. Гликопротеин гаптоглобин, вступающий в комплекс с гемоглобином для предупреждения его выделения почками, тоже имеет печёночное происхождение. Данное соединение принадлежит к белкам острой фазы воспаления, обладает пероксидазной активностью. Церулоплазмин, также являющийся гликопротеином, синтезируемым печенью, можно считать внеклеточной супероксиддисмутазой, что позволяет защищать мембраны клеток; мало того, он стимулирует продукцию антител. Подобным действием, только на клеточный иммунитет, обладает трансферрин, полимеризация которого так же осуществляется гепатоцитами.
Ещё один углеводсодержащий белок, но с иммуносупрессивными свойствами, способен синтезироваться печенью - б-фетопротеин, рост концентрации которого в плазме крови служит ценным маркёром некоторых опухолей печени, яичек и яичников. Печень - источник большей части протеинов системы комплемента.
В печени наиболее активно протекает обмен мономеров белков - аминокислот: синтез заменимых аминокислот, синтез небелковых азотистых соединений из аминокислот (креатина, глутатиона, никотиновой кислоты, пуринов и пиримидинов, порфиринов, дипептидов, коферментов пантотената и др.), окисление аминокислот с образованием аммиака, который обезвреживается в печени при синтезе мочевины .
Итак, рассмотрим общие пути обмена аминокислот . Общие пути превращения аминокислот в печени включают реакции дезаминирования, трансаминирования, декарбоксилирования и биосинтез аминокислот.
Дезаминирование аминокислот. Доказано существование 4 типов дезаминирования аминокислот (отщепление аминогруппы) (приложение 17). Выделены соответствующие ферментные системы, катализирующие эти реакции, и идентифицированы продукты реакции. Во всех случаях NH 2 -группа аминокислоты освобождается в виде аммиака. Помимо аммиака, продуктами дезаминирования являются жирные кислоты, оксикислоты и кетокислоты.
Трансаминирование аминокислот. Под трансаминированием подразумевают реакции межмолекулярного переноса аминогруппы (NH2—) от аминокислоты на б-кетокислоту без промежуточного образования аммиака. Реакции трансаминирования являются обратимыми и протекают при участии специфических ферментов аминотрансфераз, или трансаминаз.
Пример реакции трансаминирования:
Декарбоксилирование аминокислот. Процесс отщепления карбоксильной группы аминокислот в виде СО 2 . Образующиеся продукты реакции - биогенные амины. Реакции декарбоксилирования в отличие от других процессов промежуточного обмена аминокислот являются необратимыми. Они катализируются специфическими ферментами - декарбоксилазами аминокислот.
Обезвреживание аммиака в организме . В организме человека подвергается распаду около 70 г аминокислот в сутки, при этом в результате реакций дезаминирования и окисления биогенных аминов освобождается большое количество аммиака, являющегося высокотоксичным соединением. Поэтому концентрация аммиака в организме должна сохраняться на низком уровне. Уровень аммиака в крови в норме не превышает 60 мкмоль/л. Аммиак должен подвергаться связыванию в печени с образованием нетоксичных соединений, легко выделяющихся с мочой.
Один из путей связывания и обезвреживания аммиака в организме это биосинтез глутамина (и, возможно, аспарагина). Глутамин и аспарагин выделяются с мочой в небольшом количестве. Скорее они выполняют транспортную функцию переноса аммиака в нетоксичной форме. Синтеза глутамина, катализируется глутаминсинтетазой.
Второй и основной путь обезвреживания аммиака в печени - образование мочевины, который будет рассмотрен ниже в мочевинообразовательной функции печени.
В гепатоцитах отдельные аминокислоты подвергаются специфическим преобразованиям. Из серосодержащих аминокислот образуется таурин, который позднее включается в парные жёлчные кислоты (таурохолевая, тауродезоксихолевая), а также может служить антиоксидантом, связывая гипохлорит анион, стабилизировать мембраны клеток; происходит активация метионина, который в виде S - аденозилметионина служит источником метильных групп реакциях окончания генеза креатина, синтеза холина для холинфосфатидов (липотропных веществ).
Биосинтез заменимых аминокислот. Любая из заменимых аминокислот может синтезироваться в организме в необходимых количествах. При этом углеродная часть аминокислоты образуется из глюкозы, а аминогруппа вводится из других аминокислот путем трансаминирования. Алании, аспартат, глутамат образуются из пирувата, оксалоацетата и б-кетоглутарата соответственно. Глутамин образуется из глутаминовой кислоты при действии глутаминсинтетазы:
Аспарагин синтезируется из аспарагиновой кислоты и глутамина, который служит донором амидной группы; реакцию катализирует аспарагинсинтетаза пролин образуется из глутаминовой кислоты. Гистидин (частично заменимая аминокислота) синтезируется из АТФ и рибозы: пуриновая часть АТФ поставляет фрагмент —N=CH—NH— для имидазольного цикла гистидина; остальная часть молекулы образуется за счет рибозы.
Если в пище нет заменимой аминокислоты, клетки синтезируют ее из других веществ, и тем самым поддерживается полный набор аминокислот, необходимый для синтеза белков. Если же отсутствует хотя бы одна из незаменимых аминокислот, то прекращается синтез белков. Это объясняется тем, что в состав подавляющего большинства белков входят все 20 аминокислот; следовательно, если нет хотя бы одной из них, синтез белков невозможен.
Частично заменимые аминокислоты синтезируются в организме, однако скорость их синтеза недостаточна для обеспечения всей потребности организма в этих аминокислотах, особенно у детей. Условно заменимые аминокислоты могут синтезироваться из незаменимых: цистеин — из метионина, тирозин — из фенилаланина. Иначе говоря, цистеин и тирозин — это заменимые аминокислоты при условии достаточного поступления с пищей метионина и фенилаланина .
1.1.4 Участие печени в обмене витаминов
Участие печени в обмене витаминов складывается из процессов депонирования всех жирорастворимых витаминов: А, Д, Е, К, F (секреция желчи так же обеспечивает всасывание этих витаминов) и многих из гидровитаминов (В 12 , фолиевая кислота, В 1 , В 6 , РР и др.), синтеза некоторых витаминов (никотиновая кислота) и коферментов.
Особая печени заключается в том, что в ней происходит активация витаминов:
- Фолиевая кислота с помощью витамина С восстанавливается в тетрагидрофолиевую кислоту (ТГФК) ; Восстановление сводится к разрыву двух двойных связей и присоединению четырех водородных атомов в положениях 5, 6, 7 и 8 с образованием тетрагидрофолиевой кислоты (ТГФК). Оно протекает в 2 стадии тканях при участии специфических ферментов, содержащих восстановленный НАДФ. Сначала при действии фолатредуктазы образуется дигидрофолиевая кислота (ДГФК), которая при участии второго фермента - дигидрофолатредуктазы - восстанавливается в ТГФК:
- Витамины В 1 и В 6 фосфорилируются в тиаминдифосфат и пиридоксальфосфат соответственно . Витамин В 6 (пиридоксин) производный 3-оксипиридина. Термином витамин В 6 обозначают все три производных 3-оксипиридина, обладающих одинаковой витаминной активностью: пиридоксин (пиридоксол), пиридоксаль и пиридоксамин:
Хотя все три производных 3-оксипиридина наделены витаминными свойствами, коферментные функции выполняют только фосфорилированные производные пиридоксаля и пиридоксамина. Фосфорилирование пиридоксаля и пиридоксамина является ферментативной реакцией, протекающей при участии специфических киназ. Синтез пиридоксальфосфата, например, катализирует пиридоксалькиназа:
Витамин В 1 (тиамин). В химической структуре его содержатся два кольца - пиримидиновое и тиазоловое, соединенных метиленовой связью. Обе кольцевые системы синтезируются отдельно в виде фосфорилированных форм, затем объединяются через четвертичный атом азота.
В превращении витамина B1 в его активную форму - тиаминпирофосфат (ТПФ), называемый также тиаминдифосфатом (ТДФ), участвует специфический АТФ-зависимый фермент тиаминпирофосфокиназа.
- Часть каротинов преобразуется в витамин А под влиянием каротиндиоксигеназы. Каротины являются провитаминами для витамина А. Известны 3 типа каротинов: б-, в- и г-каротины, отличающиеся друг от друга химическим строением и биологической активностью. Наибольшей биологической активностью обладает в-каротин, поскольку он содержит два в-иононовых кольца и при распаде в организме из него образуются две молекулы витамина А:
При окислительном распаде б- и г-каротинов образуется только по одной молекуле витамина А, поскольку эти провитамины содержат по одному в-иононовому кольцу.
4. Витамин Д подвергается первому гидроксилированию на пути получения гормона кальцитриола; в печени осуществляется гидроксилирование в 25-м положении. Ферменты, катализирующие эти реакции, называются гидроксилазами, или монооксигеназами. В реакциях гидроксилирования используется молекулярный кислород.
5. Окислившийся витамин С восстанавливается в аскорбиновую кислоту;
6. Витамины РР, В 2 , пантотеновая кислота включаются в соответствующие нуклеотиды (НАД + , НАД + Ф, ФМН, ФАД, КоА-SH);
7. Витамин К окисляется, чтобы в виде своего пероксида служить коферментом в созревании (посттрансляционной модификации) белковых факторов свёртывания крови.
В печени синтезируются белки, выполняющие транспортные функции по отношению к витаминам. Например, ретинолсвязывающий белок (его содержание уменьшается при опухолях), витамин Е-связывающий белок и т.д. Часть витаминов, в первую очередь жирорастворимых, а также продуктов их преобразований выделяется из организма в составе жёлчи.
1.1.5 Участие печени в водно-минеральном обмене
Участие печени в водно-минеральном обмене состоит в том, что она дополняет деятельность почек в поддержании водно-солевого равновесия и является как бы внутренним фильтром, организма. Печень задерживает ионы Na + , К + , Сl - , Ca 2+ и воду и выделяет их в кровь. Кроме того, печень депонирует макро- (К, Na, Ca, Mg, Fe) и микро- (Cu, Mn, Zn, Cо, As, Cd, Pb, Se) элементы и участвует в их распределении по другим тканям с помощью транспортных белков.
Для накопления железа гепатоциты синтезируют специальный белок - ферритин. В ретикулоэндотелиоцитах печени и селезенки регистрируется водонерастворимый железосодержащий протеиновый комплекс - гемосидерин. В гепатоцитах синтезируется церулоплазмин, который, кроме вышеназванных функций, выполняет роль транспортного белка для ионов меди. Трансферрин, обладающий как и церулоплазмин, полифункциональностью, также образуется в печени и используется для переноса в плазме крови только ионов железа. Данный белок необходим для эмбрионального клеточного роста в период формирования печени. В печени ион Zn включается в алкогольдегидрогеназу, необходимую для биотрансформации этанола. Поступившие в гепатоциты соединения селена преобразуются в Se-содержащие аминокислоты и с помощью специфической т-РНК включаются в различные Se-протеины: глутатионпероксидазу (ГПО), 1-йодтиронин-5’- дейодиназу, Se-протеин Р. Последний считают основным транспортёром этого микроэлемента. Дейодиназа, обнаруженная не только в печени, обеспечивает конверсию прогормона тироксина в активную форму - трийодтиронин. Как известно, глутатионпероксидаза - ключевой фермент антирадикальной защиты. В печени сера, включённая в аминокислоты, окисляется до сульфатов, которые в виде ФАФС (фосфоаденозилфосфосульфатов) используются в реакциях сульфирования ГАГов, липидов, а также в процессах биотрансформации ксенобиотиков и некоторых эндогенных веществ (примеры продуктов инактивации - скатоксилсульфат, индоксилсульфат). Печень способна служить временным депо воды, особенно при отёках (количество Н 2 О может составлять до 80 % от массы органа) .
1.1.6 Участие печени в пигментном обмене
Участие печени в обмене пигментов проявляется в превращении хромопротеидов до билирубина в клетках РЭС, имеющихся в печени, конъюгации билирубина в самих печеночных клетках и разложении в них всасывающегося из кишечника уробилиногена до непигментных продуктов.
Гемохромогенные пигменты, образуются в организме при распаде гемоглобина (в значительно меньшей степени при распаде миоглобина, цитохромов и др.).
Начальным этапом распада гемоглобина (в клетках макрофагов, в частности в звездчатых ретикулоэндотелиоцитах, а также в гистиоцитах соединительной ткани любого органа) является разрыв одного метинового мостика с образованием вердоглобина. В дальнейшем от молекулы вердоглобина отщепляются атом железа и белок глобин. В результате образуется биливердин, который представляет собой цепочку из четырех пиррольных колец, связанных метановыми мостиками. Затем биливердин, восстанавливаясь, превращается в билирубин - пигмент, выделяемый с желчью и поэтому называемый желчным пигментом. Образовавшийся билирубин называется непрямым (неконъюгированным) билирубином. Он нерастворим в воде, дает непрямую реакцию с диазореактивом, т.е. реакция протекает только после предварительной обработки спиртом. В печени билирубин соединяется (конъюгирует) с глюкуроновой кислотой. Эта реакция катализируется ферментом УДФ-глюкуронилтрансферазой, при этом глюкуроновая кислота вступает в реакцию в активной форме, т.е. в виде УДФГК. Образующийся глюкуронид билирубина получил название прямого билирубина (конъюгированный билирубин). Он растворим в воде и дает прямую реакцию с диазореактивом. Большая часть билирубина соединяется с двумя молекулами глюкуроновой кислоты, образуя диглюкуронид билирубина. Образовавшийся в печени прямой билирубин вместе с очень небольшой частью непрямого билирубина выводится с желчью в тонкую кишку. Здесь от прямого билирубина отщепляется глюкуроновая кислота и происходит его восстановление с последовательным образованием мезобилирубина и мезобилиногена (уробилиногена). Из тонкой кишки часть образовавшегося мезобилиногена (уробилиногена) резорбируется через кишечную стенку, попадает в воротную вену и током крови переносится в печень, где расщепляется полностью до ди- и трипирролов. Таким образом, в норме в общий круг кровообращения и мочу мезобилиноген не попадает. Основное количество мезобилиногена из тонкой кишки поступает в толстую и здесь восстанавливается до стеркобилиногена при участии анаэробной микрофлоры. Образовавшийся стеркобилиноген в нижних отделах толстой кишки (в основном в прямой кишке) окисляется до стеркобилина и выделяется с калом. Лишь небольшая часть стеркобилиногена всасывается в систему нижней полой вены (попадает сначала в геморроидальные вены) и в дальнейшем выводится с мочой (приложение 18).
В большинстве случаев заболеваний печени клинические тесты уточняют характер поражения, основываясь на принципах синдромальной диагностики. Основные патологические процессы объединяют в лабораторные синдромы с учётом индикаторных тестов: 1) цитолиза; 2) холестаза (внутри- и внепечёночного); 3) гепатодепрессии (печёночно-клеточной недостаточности, малой недостаточности печени, недостаточности синтетических процессов); 4) воспаления; 5) шунтирования печени; 6) регенерации и опухолевого роста.
При подозрении на конкретную патологию учитываются основные биохимические синдромы, характерные для данного заболевания. За основу берётся стандартная программа функционального обследования, но по каждому случаю исследуется не менее двух тестов .
2.2.1 Синдром цитолиза
Возникает при повреждении клеток печени и протекает на фоне выраженного нарушения целостности мембран гепатоцитов и их органелл, приводящих к выделению составных частей клеток в межклеточное пространство и кровь. Подвергающаяся цитолизу клетка чаще сохраняет свою жизнеспособность, если же она погибает, то говорят о некрозе.
При патологии гепатоцитов ферменты, освобождающиеся из них, быстро оказываются в плазме крови, так как клетки печени имеют прямой контакт с интерстициальным и внутрисосудистым пространством, кроме того, проницаемость стенок капилляров в этом органе высока.
Главные биохимические сдвиги отмечаются в общих путях катаболизма. Страдает окислительное фосфорилирование, в результате падает уровень АТФ, изменяется концентрация электролитов. Дисбаланс последних отражается на степени проницаемости клеточных мембран. Длительное угнетение синтеза АТФ приводит к дефициту энергии, повреждению синтеза белка, мочевины и гиппуровой кислоты, наблюдаются изменения в липидном и углеводном обменах.
Важную роль в прогрессировании этого состояния играют лизосомы, которые разрушаются из-за распада мембранных структур, и в цитозоль выходят гидролитические ферменты.
Данный лабораторный синдром чаще встречается при остром вирусном гепатите и других острых повреждениях печени (лекарственных, токсических), хронических активных гепатитах, циррозах, при быстро развивающейся и длительной подпечёночной желтухе .
2.2.2 Синдром холестаза
Обусловлен сдвигами в жёлчевыделительной функции печёночных клеток с нарушением образования жёлчной мицеллы и поражением мельчайших жёлчных ходов при внутрипечёночном холестазе. Внепечёночный холестаз связан с механическими препятствиями для нормального оттока жёлчи во внепечёночных жёлчных путях.
При синдроме холестаза повышается активности экскреторных ферментов, наблюдается гиперхолестеринемия, увеличивается содержание фосфолипидов, липопротеидов низкой плотности (ЛПНП), солей жёлчных кислот. Возможна гипербилирубинемия за счёт связанной фракции, уменьшается концентрации альбуминов и увеличивается содержания б, в- и г-глобулинов в сыворотке крови.
При синдроме холестаза важное диагностическое значение имеет определение активности щелочной фосфатазы, которая отщепляет остаток фосфорной кислоты от её органических эфиров. Это гетерогенный фермент, который представлен различными изомерами, т. к. при синдроме отмечается максимальный рост щелочной фосфатазы. Определение активности лейцинаминопептидазы (ЛАП), гидролизующей N-концевые остатки аминокислот в белках так же важно при холестазе. При вирусном гепатите активность ЛАП, как и аминотрансфераз, усилена (и в 100 раз может превышать верхнюю границу физиологического уровня).
У больных холестатическими формами повреждения печени регистрируются сдвиги пигментного обмена. В частности, отмечается гипербилирубинемия, обусловленная связанной его формой. Билирубин за счёт своей гидрофильности появляется в моче, придавая ей тёмную окраску. С другой стороны, в моче отсутствует уробилин. Характерным диагностическим признаком является наличие солей жёлчных кислот в моче, которые придают ей пенистость .
2.2.3 Синдром гепатодепрессии (малой недостаточности печени)
В основном характеризуется нарушением синтетической функции. При синдроме наблюдается понижение активности холинэстеразы в сыворотке крови, количественные сдвиги уровня глюкозы крови, уменьшение содержания общего белка, особенно альбуминов, гипохолестеринемия, падение значений II, V, VII факторов свёртывания крови, гипербилирубинемия за счёт роста вклада свободной фракции, изменение параметров нагрузочных проб (бромсульфалеиновой по Розенталю-Уайту, индоциановой-вофавердиновой, уевердиновой, антипириновой, галактозной, кофеиновой).
По диагностической ценности гепатодепрессивный синдром значительно уступает цитолитическому. Однако биохимические индикаторы этого страдания играют важную роль для определения тяжести заболевания и выявления тяжёлой печёночно-клеточной недостаточности, характерной для молниеносных форм. Наиболее чувствительными критериями являются антипириновая проба, содержание проконвертина в сыворотке крови (в норме 80-120%), которые у большинства больных с синдромом гепатодепрессии со средней степенью тяжести снижены. В повседневной практике пока широко используются тесты средней чувствительности - протромбиновый индекс и активность холинэстеразы (ХЭ) в сыворотке крови. В организме человека определяют два вида ХЭ: истинную ацетилхолинэстеразу и псевдохолинэстеразу. Первая гидролизует ацетилхолин, и ею богаты нервная ткань и эритроциты, вторая синтезируется в основном в гепатоцитах и расщепляет как холиновые, так и нехолиновые эфиры. Активность ХЭ является важным лабораторно-диагностическим параметром, характеризующим функциональное состояние печени. При данном синдроме активность ХЭ угнетается. К тестам этой группы примыкает определение содержания глюкозы. Установлено, что чем тяжелее течение острого гепатита, тем чаще наблюдается гипогликемия. При острой печёночной недостаточности снижение уровня этого моносахарида в крови развивается у каждого четвертого пациента.
Дисбаланс белкового спектра сыворотки крови характеризуется гипоальбуминемией и повышением величин глобулинов за счет г-фракции. При лёгкой форме гепатита количество протеинов не изменено, при более тяжёлых - отмечается гиперпротеинемия на фоне снижения цифр альбуминов. Вторичная гипоальбуминемия при хронических поражениях печени (тяжелом длительном вирусном гепатите, ЦП) служит неблагоприятным прогностическим признаком. Она может привести к падению онкотического давления плазмы крови, развитию отёков, и впоследствии к асциту.
Нарушения липидного обмена, а именно, гипохолестеринемия особенно для эфиросвязанной фракции, отмечаются при остром вирусном гепатите, злокачественных опухолях печени. Наибольшее диагностическое значение имеет определение фракционного состава холестерина и отдельных липопротеинов (прежде всего ЛПВП) плазмы крови .
Изменения пигментного обмена при нарушении функции части печёночных клеток характеризуются гипербилирубинемией за счёт свободного билирубина. В зависимости от уровня метаболического блока выделяют повреждения на следующих этапах: в активном транспорте свободной фракции из крови в клетки печени и в образовании билирубинглюкуронидов в гепатоцитах.
2.2.4 Синдром воспаления
Обусловлен сенсибилизацией клеток иммунокомпетентной ткани и активацией ретикулогистиоцитарной системы. Гистологическим выражением этого синдрома является лимфо-макрофагальная инфильтрация портальных трактов и внутридольковой стромы, то есть иммунное воспаление. Любая иммунологическая реакция развёртывается при взаимодействии Т- и В-лимфоцитов, макрофагов, нейтрофилов. При алкогольных поражениях печени в процесс вовлекаются эозинофилы. Для синдрома воспаления характерно: гиперпротеинемия за счёт роста в основном доли г-глобулинов, повышение величин иммуноглобулинов, особенно IgG, IgM, IgA, изменение белково-осадочных проб (тимоловой, сулемовой, Вельтмана), появление неспецифических антител к дезоксирибо-нуклеопротеидам, гладкомышечным волокнам, митохондриям, микросомам.В клинико-диагностических лабораториях находят широкое применение пробы на коллоидную устойчивость (тимоловая, проба Вельтмана, цинк-сульфатная). Положительный результат этих тестов обусловлен количественными изменениями в содержании отдельных фракций (б-, в-, г-глобулинов) либо снижением соотношения альбумины/глобулины. Наибольшее распространение получила проба Маклагана (тимоловая), которая четко регистрируется в 90% случаев острого вирусного гепатита ещё в преджелтушной стадии заболевания, а также и при безжелтушной его форме.
Регистрируется за счёт развития мощных венозных коллатералей с последующим поступлением в общий кровоток большого количества веществ, которые в норме должны были трансформироваться в печени. К этим соединениям принадлежат соли аммония, фенолы, аминокислоты (тирозин, фенилаланин, триптофан, метионин), жирные кислоты с короткой цепью, содержащие 4-8 атомов углерода (масляная, валериановая, капроновая и каприловая кислоты) и меркаптаны. Накапливаясь в крови в больших концентрациях, они становятся токсичными для центральной нервной системы и угрожают возникновением печёночной энцефалопатии. К веществам этой группы относят также эндотоксины - липополисахариды грамотрицательных кишечных микробов .
При заболеваниях печени, особенно при циррозе, нарушены процессы дезаминирования аминокислот, синтеза мочевины. Аминный азот крови не способен обезвреживаться в печени (за счёт преобразования в мочевину) и направляется в общий круг кровообращения, где высокая его концентрация вызывает токсический эффект. «Аммиачная» интоксикация - один из важнейших симптомов, стимулирующих развитие «печёночной» комы и энцефалопатии .
2.2.6 Синдром регенерации и опухлевого роста печени
Его индикатором является обнаружение в сыворотке крови больших количеств б-фетопротеина (в 8 раз и более по сравнению с нормой). Малые повышения уровня этого гликопротеина (в 1,5-4 раза) чаще встречаются при усилении регенерации, в частности при активном циррозе печени. Вообще, переход синдрома в хронический гепатит, далее в цирроз и рак можно рассматривать как единый патологический процесс.
Заключение
Печень является одним из наиболее важных органов, поддерживающих жизнедеятельность организма, так как биохимические функции, включающие различные обменные реакции, протекающие в печени, - основа и связующее ядро общего метаболизма веществ. Кроме того, печень выполняет специфические функции, например, участвует в пищеварении, секретируя желчь; фильтрует кровь с образованием конечных продуктов обмена веществ, которые в дальнейшем выводятся из организма; частично обеспечивает иммунитет, синтезируя белки плазмы крови.
В общем все функции печени ведут к поддержанию гомеостаза и нарушение хотя бы одной из них может повлечь изменения во всем организме, это значит, что заболевания печени влияют на состояние остальных органов и организма в целом. Поэтому в курсовой работе было рассмотрено нормальное и патологическое состояние печени и были затронуты основы лабораторной диагностики, так как знание навыков определения синдромов поражения печени позволяет в дальнейшем точно поставить диагноз и определить причину заболевания, что очень важно на ранней стадии и дает возможность назначить соответствующее лечение.
Список литературы
1. Анохин, П.К. Нейрофизиологическая теория голода, аппетита и насыщения [Электронный ресурс] / Анохин П. К., Судаков К.В. - 1971.- т. 2, № 1. - с. 3. - режим доступа: http://www.curemed.ru/medarticle/articles/14248.htm.
2. Березов, Т.Т. Биологическая химия [Текст]: учебник / Т. Т. Березов, Б. Ф. Коровкин. - 3-е изд., перераб и доп. - М.: Медицина, 1998. - 704 с.: ил. - (Учеб. лит. Для студентов мед вузов). - ISBN 5-225-02709-1.
3. Биохимия [Текст]: учебник для вузов / под ред. чл.-корр. РАН, проф. Е. С. Северина. - 2-е изд., испр. - М.: ГЭОТАР-МЕД, 2004. - 748 с.: ил. - (серия «XXI век»). - ISBN 5-9231-0390-7.
4. Клиническая биохимия [Текст] / под ред. чл. корр. РАН, акад РАМН В. А. Ткачука. - 2-е изд., испр и доп. - М.: ГЭОТАР-МЕД, 2004. - 512 с. - (Классический университетский учебник). - ISBN 5-9231-0420-2.
5. Марри, Р. Биохимия человека [Текст]: в 2-х томах / Р. Марри, Д. Греннер, П. Мейес, В. Родуэлл. - пер. с англ. В. В. Борисова, Е. В. Дайниченко; под ред. Л.М. Гинодмана. - М.: Мир, 1993. - ил. - ISBN 5-03-001774-7.
6. Никитина, Л.П. Биохимия печени в норме и при патологии [Текст]: учебное пособие для преподавателей и студентов медицинских вузов, врачей, интернов, клинических ординаторов / Л.П.Никитина, Н.В.Соловьева,
П.Б.Цидендамбаев. - Чита: ГОУ ЧГМА, 2004. - 52 с.
7. Николаев, А.Я. Биологическая химия [Текст] / А.Я. Николаев. - 4-е изд., перераб. и доп. - М.: Медицинское информационное агенство. - 2004. - 556 с.: ил. - ISBN 5-89481-219-4.
8. Страйер, Л. Биохимия [Текст]: в 3-х томах / Л. Страйер. - пер. с англ. М. Д. Гроздовой; под ред. С.Е. Северина. - М.: Мир, 1984. - ил.
 Как сделать забор в майнкрафте 1
Как сделать забор в майнкрафте 1 Оригинальный декор из лампочек своими руками
Оригинальный декор из лампочек своими руками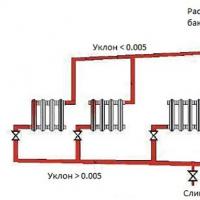 Расширительный бак для отопления
Расширительный бак для отопления Ворота и калитки для панельных ограждений
Ворота и калитки для панельных ограждений Снип 2 04 03 85 рекомендации
Снип 2 04 03 85 рекомендации Водородная вода: польза и вред, какой купить генератор и как сделать в домашних условиях Генератор водородной воды: какой лучше
Водородная вода: польза и вред, какой купить генератор и как сделать в домашних условиях Генератор водородной воды: какой лучше Сделаем качественный капитальный ремонт квартир под ключ: недорого и с гарантией
Сделаем качественный капитальный ремонт квартир под ключ: недорого и с гарантией