Органические соединения. Реакция поликонденсации Мономеры, способные к поликонденсации
HOOC–CH 2 –NH 2 + HOOC–CH–NH 2 HOOC–CH 2 –NH–CO–CH–NH 2
CH 3 –H 2 O CH 3
глицин аланин глицилаланин пептидная связь
(гли-ала)
Ди-, три-, ….полипептиды называют по наименованию аминокислот, составляющих полипептид, в котором все входящие аминокислоты в качестве радикалов заканчиваются на –ил , а последняя аминокислота звучит в названии без изменения.
Поликонденсацией ε - аминокапроновой кислоты или полимеризацией капролактама (лактам ε – капроновой кислоты) получают смолу капрон:
N CH 2 CH 2 [– NH – (CH 2) 5 – CO – NH – (CH 2) 5 – CO –] m
капролактам поликапролактам (капрон)
Эта смола применяется в производстве синтетического капронового волокна.
Другой пример синтетического волокна – это энант.
Энант представляет собой полиамид энантовой кислоты. Получают энант поликонденсацией 7-аминогептановой кислоты, находящейся в реакции в виде внутренней соли:
N N + H 3 – (CH 2) 6 – COO – [ – NH – (CH 2) 6 – CO – ] n + n H 2 O
Энант применяется для изготовления синтетического волокна, в получении «искусственного» меха, кожи, пластмасс и др. Для энантовых волокон характерны большая прочность, легкость и упругость.
Тесты для самоконтроля знаний по теме: «Аминокислоты»
1. Назвать соединение по систематической номенклатуре
СН 3 – СН – СООН
A) 2-аминопропановая кислота
B) a-аминопропионовая кислота
C) a-аланин
D) 2-аминопропионовая кислота
2. Назвать соединение по исторической номенклатуре
СН 3 – СН – СН – СООН
A) a–амино - b– метилмаслянная кислота
B) a–метил - b– аминомаслянная кислота
C) 2-амино- 3 – метилбутановая кислота
D) 2-метил – 3 – аминобутановая кислота
3. Аланин Н NH 2 относится к ряду
4. Продуктами реакций является
СН 2 – СООН PCl 5 B
NH 2 NH 3 C
A) A: CH 2 – COONa; B: CH 2 – COCl; C: CH 2 – CONH 2
B) A: CH 2 – COONa; B: CH 2 – COCl 2 ; C: CH 2 – CONH 4
C) A: CH 2 – COONa; B: CH 2 – COOH; C: CH – NH 2
D) A: CH 2 – COONa; B: CH 2 – COOH; C: CH 2 – CONH 2
NH 2 N + H 3 Cl – NH 2
5. Продуктами реакций является
СН 2 – СООН CH 3 Br B
NH 2 CH 3 COCl C
HNO 2 Д
A) A: CH 2 – COOH; B: CH 2 – COOH; C: CH 2 – COOH; Д: CH 2 - COOH
N + H 3 Cl – NHCH 3 NH – COCH 3 OH
B) A: CH 2 – COOCl; B: CH 2 – COOCH 3 ; C: CH 2 – COOH; Д: CH 2 - COOH
NH 2 NH 2 NH-COCH 3 ; OH
C) A: CH 2 – COCl 2 ; B: CH 2 – COOH; C: CH 2 – COOH; Д: CH 2 - COOH
NH 2 NH-CH 3 NH – COCH 3 NH-N = O
D) A: CH 2 – COCl 2 ; B: CH 2 – COBr; C: CH 2 – COOH; Д: CH 2 - COOH
NH 2 NH 2 NH – COCH 3 OH
6. a-Аминокислоты при нагревании образуют
A) лактамы
B) кетопиперазины
C) лактoны
D) лактиды
7. b-аминокислоты при нагревании образуют
A) непредельные кислоты
B) кетопиперазины
C) лактамы
D) лактоны
8. g-аминокислоты при нагревании образуют
A) лактамы
B) непредельные кислоты
C) лактиды
D) лактоны
9. При поликонденсации аминокислот образуются
A) пептиды
C) пиперазины
D) полиены
10. Пептидная связь в молекулах белка – это
11. Поликонденсация отличается от полимеризации:
A) Отсутствием образования побочных низкомолекулярных продуктов
B) Образованием побочных низкомолекулярных продуктов
C) Окислением
D) Разложением
12. Качественной реакцией на a-аминокислоты является реакция c:
A) нингидрином
B) a-нафтолом
13. Назвато продукты реакций в синтезе Штрекера-Зелинского:
CH 3 HCN NH 3 2 HOH (HCl)
CH = O А В С
А) А- α-оксинитрил масляной кислоты; В- α-аминонитрил масляной кислоты;С-
D, L –аланин;
В) А- α-оксинитрил пропионовой кислоты; В- α-аминонитрил аминопропионовой кислоты;С-D, L –аланин;
С) А- α-оксинитрил валерьяновой кислоты; В- α-аминонитрил валерьяновой кислоты;
С-D, L –треонин;
D) А- α-оксинитрил пропионовой кислоты; В- α-аминонитрил пропионовой кислоты;С-
D, L –аланин.
14. Назвать вещества в цепочке превращений:
COOC 2 H 5 O=N-OH [H] (CH 3 CO) 2 O C 2 H 5 ONa
CH 2 –H 2 O А – H 2 O В –CH 3 COOH С –C 2 H 5 OH Д
малоновый эфир
Cl-CH 2 -CH(CH 3) 2 Н 2 О (НСl) t 0
–NaCl Е –CH 3 COOH, Ж – CO 2 З
–2C 2 H 5 OH
А) А-нитрозомалоновый эфир; В –оксиммалоновый эфир; С-N-ацетилоксиммалоновый эфир; Д-Na-N-ацетилоксиммалоновый эфир; Е-изобутил-N-ацетилоксиммалоновый эфир; Ж- изобутилоксиммалоновый эфир; З-изолейцин;
В) А-нитрозомалоновый эфир; В –иминомалоновый эфир; С-N-ацетилиминомалоновый эфир; Д-Na-N-ацетилиминомалоновый эфир; Е-изобутил-N-ацетилиминомалоновый эфир; Ж- изобутилиминомалоновый эфир; З-треонин;
С) А-нитрозомалоновый эфир; В –аминомалоновый эфир; С-N-ацетиламиномалоновый эфир; Д-Na-N-ацетиламиномалоновый эфир; Е-изобутил-N-ацетиламиномалоновый эфир; Ж- изобутиламиномалоновый эфир; З-лейцин;
D) А-оксиммалоновый эфир; В –нитрозомалоновый эфир; С-N-ацетилнитрозомалоновый эфир; Д-Na-N-ацетилнитрозомалоновый эфир; Е-изобутил-N-ацетилнитрозомалоновый эфир; Ж- изобутилнитрозомалоновый эфир; З-валин.
УГЛЕВОДЫ
Углеводы представляют собой большую группу органических веществ, широко распространенных в природе. Это глюкоза, сахароза, крахмал, целлюлоза и так далее.
Ежегодно растениями на нашей планете создается огромная масса углеводов, которая оценивается содержанием углерода 4 * 10 10 тонн. Около 80% сухого вещества растений приходится на углеводы и 20 – 30% - животные организмы.
Термин «углеводы» предложен в 1844 г. К. Шмидтом, так как большинству этих веществ соответствует формула С n (H 2 O) m . Например, молекула глюкозы имеет формулу С 6 Н 12 О 6 и равно 6 атомам углерода и 6 молекулам воды. Позднее были найдены углеводы, не соответствующие этому составу, например, дезоксигексоза (С 6 Н 10 О 5), но термин сохранился до сих пор.
Углеводы делятся на две большие группы – это простые углеводы или моносахариды (монозы), вещества, не подвергающиеся гидролизу, например, глюкоза, фруктоза. В природе больше распространены пентозы и гексозы. Вторая группа – это сложные углеводы, которые при гидролизе дают моносахариды. Сложные углеводы, в свою очередь, делятся на олигосахариды и полисахариды. Олигосахариды состоят от двух до десяти остатков моноз. «Олигос» в переводе означает «немногие». Простейшими олигосахаридами являются дисахариды (биозы), состоящие из двух остатков моноз. Например, сахароза С 6 Н 12 О 6 состоит из остатков двух моноз: глюкозы и фруктозы. Олигосахариды, состоящие из остатков трех моноз, называются триозами, из четырех – тетраозами и так далее. Полисахариды (полиозы) образуются из моноз в результате их поликонденсации., то есть полиозы – это гетероцепные полимеры или биополимеры, мономерами которых являются монозы. Гетероцепные полимеры содержат в своей цепи не только атомы углерода, но и атомы кислорода, например:
NC 6 H 12 O 6 (C 6 H 10 O 5) n + (n-1)H 2 O или (-C 6 H 10 O 4 – O -) n
Углеводы
5.3. ПОЛИКОНДЕНСАЦИЯ
Поликонденсация - это реакция образования макромолекул при соединении мономеров между собой, сопровождающаяся отщеплением простых веществ - воды, спирта, аммиака, хлористого водорода и т.п. При поликонденсации протекает ряд кинетически не связанных бимолекулярных реакций. Особенности реакции поликонденсации:
- 1) элементарный состав звена полимера отличается от состава исходного мономера;
- 2) мономерные звенья в молекуле полимера связаны между собой ковалентной или семиполярной связью;
- 3) в результате реакции образуются полимерные цепи различной длины, т.е. продукт полидисперсен;
- 4) поликонденсация - ступенчатый процесс.
Таблица 5.4. Типы соединений, образующихся при поликонденсации, в зависимости от природы функциональных групп
| Первая функциональная группа (а) | Вторая функциональная группа (b) | Исходное вещество | Тип образующегося соединения |
| -H | H- | Углеводород | Полиуглеводород |
| -H | Сl- | Галогенпроизводное | То же |
| -Вr | Вr- | Дигалогенпроизводное | " |
| -ОН | НО- | Многоатомный спирт | Полиэфир простой |
| -OH | HOOC- | Оксикислота | Полиэфир сложный |
| -OH | ROOC- | Эфир оксикислоты | То же |
| -NH 2 | НООС- | Аминокислота | Полиамид |
| -NH 2 | ROOC- | Эфир аминокислоты | То же |
| -NH 2 | СlОC- | Хлорангидрид аминокислоты | " |
В процессе поликонденсации могут участвовать как однородные, так и разнородные молекулы. В общем виде эти реакции изображены следующими схемами:
- х а-А-b → а-(А) х -b + (х - 1)ab;
- х а-А-а + x b-B-b → a-(A-B)-b + 2(х - 1)ab,
где а и b - функциональные группы.
Свойства продукта, образующегося при поликонденсации, определяются функциональностью мономера, т.е. числом реакционноспособных функциональных групп. Реакция поликонденсации может быть использована для синтеза различных классов как карбоцепных, так и гетероцепных полимеров.
При поликонденсации бифункциональных соединений образуются линейные полимеры (табл. 5.4). Если функциональность мономера больше двух, то образуются разветвленные и трехмерные полимеры. Количество функциональных групп в макромолекуле при этом возрастает по мере углубления реакции. Для синтеза волокнообразующих полимеров наибольший интерес представляют бифункциональные соединения.
В зависимости от природы функциональных групп и строения образующегося полимера в реакции поликонденсации могут быть представлены различные классы химических реакций: полиэтерификация, полиангидридизация, полиамидирование и т.д. В табл. 5.5 приведены примеры различных типов соединений, образующихся при поликонденсации.
Взаимодействие функциональных групп мономера может приводить к образованию полимера или низкомолекулярных продуктов циклического строения. Так, например, γ-аминомасляная
Таблица 5.5. Функциональные группы и типы соединений, образующихся при поликонденсации
Таблица 5.5. (продолжение)

Таблица 5.5. (окончание)

кислота неспособна к поликонденсации вследствие образования устойчивого пятичленного цикла - лактама:
Однако ζ-аминоэнантовая кислота образует в результате дегидратации линейный полимер:
Увеличение расстояния между функциональными группами повышает вероятность образования макромолекул. Циклизация как основное направление реакции происходит лишь в тех случаях, когда должны образовываться малонапряженные пяти- и шестичленные циклы.
Вопрос. Глицин (аминоуксусная кислота) в обычных условиях неспособен к конденсации. Объясните вероятную причину этого явления.
Ответ . При взаимодействии двух молекул глицина получается ненапряженный шестичленный дикетипиперазиновый цикл по схеме

При этом в обычных условиях синтеза полимер не образуется.
В зависимости от строения исходных веществ и способа проведения реакции возможны два варианта поликонденсационных процессов: равновесная и неравновесная поликонденсация.
Равновесной поликонденсацией называется такой процесс синтеза полимера, который характеризуется небольшими значениями констант скоростей и обратимым характером превращений. Поликонденсация - многостадийный процесс, каждая ступень которого является элементарной реакцией взаимодействия функциональных групп. В качестве постулата принято считать, что реакционная способность концевых функциональных групп не изменяется при росте полимерной цепи. Процесс равновесной поликонденсации представляет собой сложную систему реакций обмена, синтеза и деструкции, которую называют поликонденсационным равновесием. В общем виде реакции поликонденсации могут быть представлены как реакции функциональных групп, например:
~СООН + НO~ ~СОО~ + Н 2 O.
Соответственно константа равновесия выражается следующим образом:
K n p =
Значение К п p постоянно на всех стадиях поликонденсации, т.е. не зависит от степени полимеризации. Так, для синтеза полиэтилентерефталата при 280°С К п р = 4,9, а полигексаметиленадипамида при 260°С К п р = 305.
Факторы, влияющие на молекулярную массу и полидисперсность поликонденсационных полимеров. Суммарную скорость процесса поликонденсации можно оценить, определяя количество функциональных групп в пробах, отобранных из реакционной смеси через различные промежутки времени. Результат выражается степенью завершенности реакции Х м, которая определяется как доля функциональных групп, прореагировавших к моменту отбора пробы.
Если N 0 - начальное число функциональных групп одного вида, a N t - число групп, не прореагировавших к моменту отбора пробы t , то
Задача. Рассчитать степень завершенности реакций поликонденсации 8-аминокапроновой кислоты, если исходное содержание карбоксильных групп составляло N 0 = 8,5 · 10 -3 экв/г, а конечное - N t = 2,4 · 10 -4 экв/г.
Решение . Схема реакции следующая:
По формуле (5.56) находим, что X м = 0,971.
Для получения полимеров с максимальной молекулярной массой берут мономеры в строго эквивалентных количествах. Каждая функциональная группа одного исходного вещества может при поликонденсации реагировать с функциональной группой другого исходного вещества.
Вместе с тем реакция синтеза полиамидов или сложных полиэфиров обычно катализируется Н + . Процесс протонирования реагирующей карбоксильной группы может быть осуществлен за счет второй группы НООС-. Поэтому скорость реакции между диамином и дикислотой или диолом и дикислотой может быть описана соответственно как
- -dC /dt = K n ;
- -dC /dt = K n [СООН][СООН][ОН].
При условии эквивалентности реагирующих функциональных групп и принимая во внимание, что = [ОН] = [НООС] = С , имеем
где С - концентрация функциональных групп; К п - константа скорости реакции.
После интегрирования при t = 0 и С = С 0 имеем
Задача. Рассчитать константу скорости реакции поликонденсации себациновой кислоты (M 0 = 202) и 2,5-толуилендиамина (M 0 = 122) , если через 40 мин реакции при 260°С концентрация карбоксильных групп составляла N t = 1,7 · 10 -4 экв/г.
Решение . Схема реакции следующая:
n НООС(СН 2) 6 СООН + n H 2 NC 6 H 3 (CH 3)NH 2 HO n H + 2(n - 1)Н 2 О.
Рассчитываем начальную концентрацию карбоксильных групп в исходной смеси, принимая во внимание, что в реакции участвуют 2 моля мономеров:
С 0 = 2/(202 + 122) = 0,61 · 10 -3 экв/г.
По формуле (5.58) определяем константу скорости реакции:
Принимая во внимание, что существенного объема системы при удалении воды не происходит [т.е. можно считать, что С t = C 0 (1 - Х м)], имеем
Задача. Определить константу скорости реакции поликонденсации адипиновой кислоты и этиленгликоля К п и выяснить, изменяется ли она с увеличением размеров молекул реагирующих веществ, если вещества взяты в эквивалентных

Рис. 5.7. Зависимость (1 - X
м) -2 от продолжительности поликонденсации t
количествах и получены следующие значения степени завершенности реакции через определенные промежутки времени:
| t , мин | 20 | 40 | 60 | 120 | 180 |
| Х м | 0,90 | 0,95 | 0,96 | 0,98 | 0,99 |
Решение. Согласно уравнению (5.59), если К п не меняется с изменением размеров реагирующих молекул, то зависимость 1/(1 - X м) 2 = f (t ) должна быть линейной. Строим график зависимости (рис. 5.7), вычислив предварительно значения 1/(1 - Х м) 2:
100; 400; 625; 2500; 1000.
Линейная зависимость (см. рис. 5.7) наблюдается лишь при небольших степенях завершенности реакции. Схема реакции следующая:
По уравнению (5.59) рассчитываем К п для t = 40 мин:
= 5,4 · 10 4 .Суммарную скорость процесса поликонденсации можно описать уравнением
где К п - константа скорости реакции поликонденсации; X м - доля функциональных групп мономера, вступивших в реакцию за время t ; a - количество низкомолекулярного продукта, образовавшегося за время t ; К п p - константа поликонденсационного равновесия.
Чтобы реакция поликонденсации была направлена в сторону образования полимера, количество низкомолекулярного продукта, находящегося в реакционной смеси, должно быть меньше
Задача. Определить константу поликонденсационного равновесия "поликонденсация - гидролиз", если при поликонденсации бензидина и пробковой кислоты за 30 мин доля карбоксильных групп, вступивших в реакцию, составляла 0,84; содержание воды в системе - 0,1 · 10 -3 моль/г; К n = 400; V = 1,3 · 10 -2 моль/(г · мин).
Решение . Схема реакции следующая:
n H 2 N(C 6 H 4) 2 NH 2 + n НООС(СН 2) 6 СООН H n OH + n H 2 O.
K n p =
= 3,3 · 10 -3 .Средняя степень полимеризации продукта поликонденсации зависит от содержания низкомолекулярного продукта реакции, изменяясь в соответствии с уравнением поликонденсационного равновесия, аналогично (6.49). Но
где п а - мольная доля низкомолекулярного продукта, выделяющегося при поликонденсации.
Задача. Определить предельно допустимое остаточное количество этиленгликоля дг в %(мас.) при реакции поликонденсации диэтиленгликольтерефталата в процессе получения полимера с молекулярной массой 20000, если К п р = 4,9.
Решение . Схема реакции следующая:

Р п = 20000/192 = 104.
По формуле (5.61) находим n a :
п а = К n p /Р 2 = 4,9/104 2 = 4,5 · 10 -4 моль/моль,
х = 4,5 · 10 -4 · 62 · 100/192 = 0,008 %(мас.).
Задача. Рассчитать среднечисленную и средневзвешенную молекулярные массы полимера, полученного при поликонденсации 4-амино-2-хлорэтилбензола, если степень завершенности реакции составляла 99,35%. Оценить полидисперсность продукта реакции.
Решение . Легко показать, что
где X м - степень завершенности реакции; М 0 - молекулярная масса мономерного звена.
Схема реакции следующая:
В соответствии с уравнением (1.70)
U = M w /M n - 1 = 1,0.
Если N 0 - начальное число функциональных групп одного вида, то степень завершенности реакции поликонденсации можно выразить следующим образом:
Решение. Схема реакции поликонденсации следующая:
Находим Х м по уравнению (5.64):
Х м = 0,0054 · 436 · 30/(2 + 0,0054 · 436 · 30) = 0,971.
Для вычисления фракционного состава продуктов поликонденсации линейных бифункциональных соединений можно в первом приближении воспользоваться уравнением Флори
где W p - массовая доля фракции полимера со степенью полимеризации Р n .
На рис. 5.8 приведены дифференциальные кривые ММР, характеризующие полидисперсность продуктов поликонденсации при различных степенях завершенности реакции Х м. Очевидно, что по мере увеличения степени превращения исходных полимеров степень полидисперсности возрастает.
Однако в результате реакций, способствующих установлению поликонденсационного равновесия, во многих случаях ММР даже при больших степенях превращения характеризуется сравнительно малыми значениями U (U

Рис.5.8. Дифференциальные кривые ММР, вычисленные по уравнению Флори (5.60) для различных степеней завершенности Х м реакции поликонденсации (числа у кривых)

Решение . Схема реакции синтеза этого полимера следующая:
По уравнению (5.65) рассчитываем W p :
- а) W p = 40 · 0,9 40-1 (1 - 0,9) 2 = 0,065;
- б) W p = 40 · 0,99 40-1 (1 - 0,99) 2 = 0,0034.
Таким образом, по мере углубления реакции содержание фракций с молекулярной массой 9000 уменьшается.
При увеличении содержания в реакционной смеси одного из видов функциональных групп молекулярная масса полимера снижается (рис. 5.9).
Оценка влияния избытка одного из видов функциональных групп в реакционной среде может быть проведена с использованием правила неэквивалентности Коршака. Согласно этому правилу,
где n ’ - число молей бифункционального соединения; т ’ - число молей монофункционального соединения.
Процессы поликонденсации можно проводить в расплаве (если мономеры и полимер достаточно устойчивы при температуре плавления полимера), в растворе, в твердой фазе, а также на поверхности раздела двух фаз (несмешивающиеся жидкости, жидкость - твердое вещество и т.д.). В условиях глубокого вакуума, обеспечивающего удаление низкомолекулярных продуктов реакции, при температуре ниже или выше T пл можно проводить реакцию дополиконденсации (соответственно в твердой или жидкой фазе).
Задание 433
Какие соединения называют аминами? Составьте схему поликонденсации адипиновой кислоты и гексаметилендиамина. Назовите образовавшийся полимер.
Решение:
Аминами
называются производные углеводородов,
образованные замещением в последних атомов водорода на группы -NH 2 , -NHR или -NR"
:
В зависимости от числа атомов водорода у атома азота, замещённых радикалами (R ), амины называются первичными, вторичными или третичными.
Группа -NH 2 , входящая в состав первичных аминов, называется аминогруппой. Группа атомов >NH во вторичных аминах называется иминогруппой .
Схема поликонденсации адипиновой кислоты и гексаметилендиамина :

Анид (найлон ) – продукт поликонденсации адипиновой кислоты и гексаметилендиамина .
Задание 442
Какие соединения называют аминокислотами? Напишите формулу простейшей аминокислоты. Составьте схему поликонденсации аминокапроновой кислоты. Как называют образующийся при этом полимер?
Решение:
Аминокислотами
называются соединения, в молекуле которых содержатся одновременно аминные
(-NH2) и карбоксильные группы
(-СООН). Простейшим представителем их является аминоуксусная кислота
(глицин
): NH2-CH2-COOH.
Схема поликонденсации аминокапроновой кислоты:

Продукт поликонденсации аминокапроновой кислоты называется капрон (перлон ). Из капрона получают волокна, превосходящие по прочности натуральные. Эти волокна применяются в производстве одежды, корда авто- и авиапокрышек, для изготовления прочных и не гниющих рыболовецких сетей и снастей, канатной продукции и т.д.
Примеры решения задач
Для получения высокомолекулярных соединений существует два основных способа: полимеризация и поликонденсация.
Полимеризация – реакция соединения молекул мономера, протекающая за счет разрыва кратных связей.
Полимеризацию можно изобразить общей схемой:
где R – заместитель, например, R = H, – СН 3 , Сl, С 6 Н 5 и др.
n – степень полимеризации.
Полимеризация алкадиенов с сопряженными двойными связями (алкадиены-1,3) протекает за счет раскрытия двойных связей в положениях 1,4 или 1,2, например:

Наиболее ценные полимеры (каучуки) получаются при стереорегулярной полимеризации в 1,4-положение в присутствии катализаторов Циглера-Натта :
Для улучшения свойств каучуков полимеризацию бутадиена-1,3 и изопрена проводят совместно со стиролом, акрилонитрилом, изобутиленом. Такие реакции называются сополимеризациями. Например,

где R = – (бутадиен – стирольный каучук),
R = -C º N (бутадиен – нитрильный каучук).
Поликонденсация – реакция образования макромолекул из ди или полифункциональных соединений, сопровождающаяся отщеплением низкомолекулярных продуктов (воды, аммиака, хлорида водорода и др.).
Поликонденсация, в которой участвует только один мономер, называется гомополиконденсацией. Например,
nНО – (СН 2) 6 – СООН (n-1)Н 2 О + Н – [–О – (СН 2) 6 –СО –]n – ОН
7-гидроксигептановая полимер
кислота (мономер)
В результате гомополиконденсации 6-аминогексановой кислоты
(e-аминокапроновой кислоты) получается полимер капрон.
Поликонденсация, в которой участвуют два мономера, содержащие различные функциональные группы, называется гетерополиконденсацией. Например поликонденсация между двухосновными кислотами и двухатомными спиртами приводит к получению полиэфиров:
nНООС – R – COOH + nHO – R¢– OH [– OC – R – COOR¢– O –]n + (2n-1) H 2 O
В результате гетерополиконденсации адипиновой кислоты и гексаметилендиамина получается полиамид (нейлон)
Пример 1.
Сколько структурных звеньев (n) входит в макромолекулу полихлорвинила с молекулярной массой 350000?
M m полимера = 350000
Определить количество структурных звеньев – (n).
1. Схема реакции:

2. Находим молекулярную массу элементарного звена ![]()
сложением атомных масс элементов, входящих в его состав – 62,5.
3. Находим (n). Делим молекулярную массу элементарного звена: 3500: 62,5 = 5600
Ответ: n = 5600
Пример 2.
Напишите схему образования димера и тримера изобутилена под действием серной кислоты с учетом механизма этой реакции (катионной полимеризации).


![]()
Такой процесс полимеризации наблюдал впервые А.М. Бутлеров при действии на изобутилен серной кислоты.
Обрыв цепи в данном случае происходит в результате отщепления протона (Н +).
Реакция идет в присутствии воды, которая захватывает протон, образуя катион гидроксония
Контрольные задания
191. Какие полимеры называют термопластичными, термореактивными?
192. Составьте уравнение реакции сополимеризации стирола
C6H5–CH=CH2и бутадиена СH2=CH–CH=СH2. Какими свойствами обладает продукт сополимеризации и где он используется?
193. Составьте уравнения реакции полимеризации пропилена
СH2=СH–CH3и изобутилена H2C=C–CH3.
194. Напишите уравнение реакции поликонденсации адипиновой кислоты HOOC(СH2)4COOH и гексаметилендиамина NH2(СH2)6NH2. Какой продукт образуется, какими свойствами обладает и где он применяется?
195. Какие углеводороды называются диеновыми? Приведите при-меры. Какой общей формулой выражают состав диеновых углеводородов? Составьте схему полимеризации одного из диеновых углеводородов.
196. Какие соединения называют аминами? Составьте схему поли-конденсации адипиновой кислоты и гексаметилендиамина. Как называют полимер, образующийся в результате этой реакции?
197. Рассчитайте молекулярную массу полихлорвинила, если степень полимеризации равна 200. Напишите уравнение реакции полимеризации хлорвинила.
198. Какие соединения называют аминокислотами? Напишите фор-мулу простейшей аминокислоты. Составьте схему поликонденсации аминокапроновой кислоты. Как называют полимер, образующийся в ре-зультате этой реакции?
199. Напишите уравнения реакций получения капрона из аминока-проновой кислоты NH2(CH2)5COOH и найлона из адипиновой кислоты COOH(CH2)4COOH и гексаметилендиамина NH2(CH2)6NH2.
200. Как называются углеводороды, представителем которых является изопрен? Составьте схему сополимеризации изопрена и изобутилена.
 Как сделать забор в майнкрафте 1
Как сделать забор в майнкрафте 1 Оригинальный декор из лампочек своими руками
Оригинальный декор из лампочек своими руками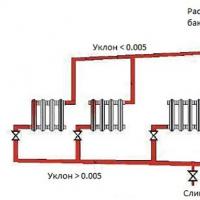 Расширительный бак для отопления
Расширительный бак для отопления Ворота и калитки для панельных ограждений
Ворота и калитки для панельных ограждений Снип 2 04 03 85 рекомендации
Снип 2 04 03 85 рекомендации Водородная вода: польза и вред, какой купить генератор и как сделать в домашних условиях Генератор водородной воды: какой лучше
Водородная вода: польза и вред, какой купить генератор и как сделать в домашних условиях Генератор водородной воды: какой лучше Сделаем качественный капитальный ремонт квартир под ключ: недорого и с гарантией
Сделаем качественный капитальный ремонт квартир под ключ: недорого и с гарантией